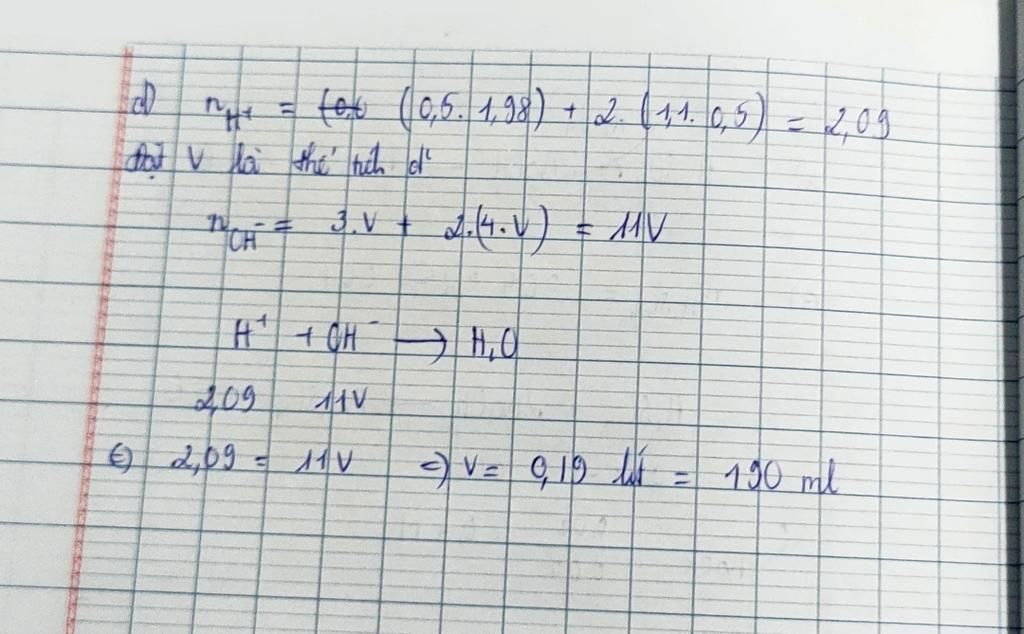Câu 3: a. Để trung hòa 40 ml dung dịch H2SO4 0,25M cần 50 ml dung dịch NaOH nồng độ x mol/l. Tính giá trị của x. b. Khi cho 100 ml dung dịch KOH 1M vào 100 ml dung dịch HCl thì phản ứng xảy ra vừa đủ. Tính nồng độ mol của HCl. Trường: THPT Phan Ngọc Hiển Hóa học 11 2 Trên bước đường thành công không có dấu chân của những kẻ lười biếng ! c. Hoà tan 17 gam hỗn hợp NaOH, KOH, Ca(OH)2 vào nước được 500 gam dung dịch X. Để trung hoà 50 gam dung dịch X cần dùng 40 gam dung dịch HCl 3,65%. Cô cạn dung dịch sau khi trung hoà thu được bao nhiêu gam muối khan? d. Lấy 500 ml dung dịch chứa đồng thời HCl 1,98M và H2SO4 1,1M trộn với V lít dung dịch chứa NaOH 3M và Ba(OH)2 4M thì trung hoà vừa đủ. Tính giá trị của V Giúp em với ạ em cảm ơn nhiều ạ
2 câu trả lời
Đáp án:
Giải thích các bước giải:
a) nH2SO4 = 0,01
H2SO4 + 2NaOH ⟶ Na2SO4 + 2H2O
0,01 ⟶ 0,02
⟹ x = 0,02/0,05 = 0,4M
b) nKOH = 0,1 = nHCl ⟹ CM HCl = 0,1/0,1 = 1 M
c) mHCl = 40.3,65:100 = 1,46 g ⟹ nHCl = 0,04
Trong 500 g X có 17 gam bazơ ⟹ 50 gam X có 1,7 gam bazơ
R(OH)n + nHCl ⟶ RCln + nH2O
0,04 ⟶ 0,04
BTKL: 1,7 + 1,46 = mmuối + 0,04.18 ⟹ mmuối = 2,44
d) nH+ = 0,5.1,98 + 0,5.1,1.2 = 2,09 mol
nOH- = V.3 + V.4.2 = 11V
Pư vừa đủ ⟹ nH+ = nOH- ⟹ 2,09 = 11V ⟹ V = 0,19