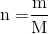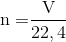Đốt cháy hoàn toàn 1,12 lít khí CH4 (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được sản phẩm là khí cacbonic (CO2) và nước (H2O). Giá trị của V là
Trả lời bởi giáo viên
Số mol khí CH4 phản ứng là: ${n_{C{H_4}}} = \dfrac{{1,12}}{{22,4}} = 0,05\,mol$
PTHH: CH4 + 2O2 $\xrightarrow{{{t^o}}}$ CO2 + 2H2O
Tỉ lệ theo PT: 1mol 2mol 1mol 2mol
0,05mol ?mol
Từ PTHH, ta có: ${n_{{O_2}}} = \dfrac{{0,05.2}}{1} = 0,1\,mol$
=> thể tích khí O2 cần dùng là: ${V_{{O_2}}} = 22,4.n = 22,4.0,1 = 2,24$ lít
Hướng dẫn giải:
+) Tính số mol khí CH4 phản ứng: ${n_{C{H_4}}} = \dfrac{{1,12}}{{22,4}}$
PTHH: CH4 + 2O2 $\xrightarrow{{{t^o}}}$ CO2 + 2H2O
Tỉ lệ theo PT: 1mol 2mol 1mol 2mol
0,05mol ?mol
Từ PTHH, ta có: ${n_{{O_2}}} = \dfrac{{0,05.2}}{1}$ => thể tích khí O2 : V = 22,4.n