V. Bài toán có lượng chất dư: Bài 1. Cho 180 gam dung dịch H2SO4 15% vào 320 gam dung dịch BaCl2 10%. Tính nồng độ % các chất trong dung dịch thu được sau phản ứng? Bài 2.Cho 200ml dung dịch Ba(OH)2 0,4M vào 250ml dung dịch H2SO4 0,3M.Tính khối lượng kết tủa thu được Giúp mình với ạ, mình cảm ơn trước ạ😊
2 câu trả lời
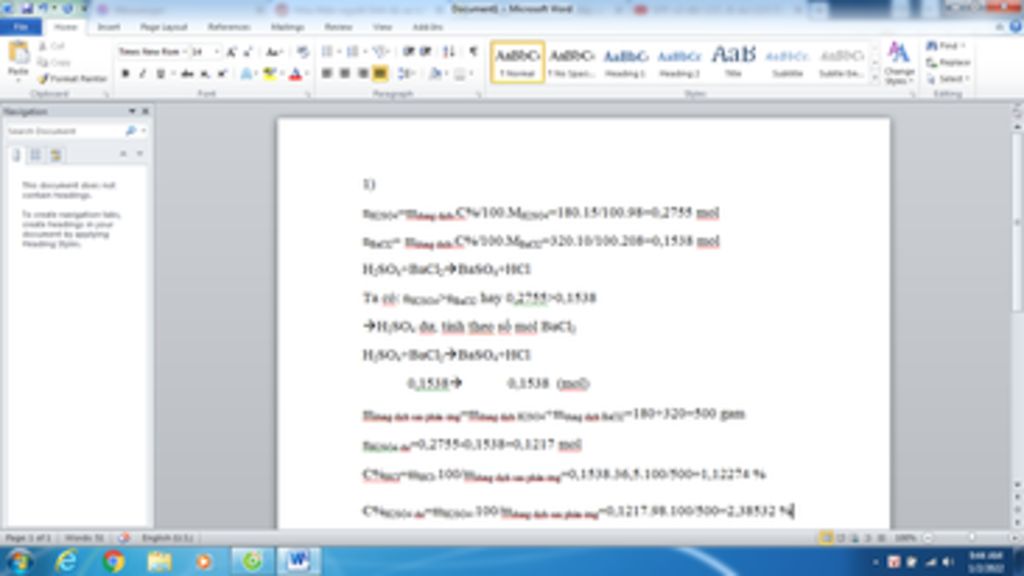
Bài 1:
$n_{H_2SO_4}=\dfrac{180.15\%}{100\%.98}\approx 0,275(mol)\\ n_{BaCl_2}=\dfrac{320.10\%}{100\%.208}\approx 0,15(mol)\\ PTHH:BaCl_2+H_2SO_4\to BaSO_4\downarrow+2HCl\\ \text{Lập tỉ lệ: }\dfrac{0,275}{1}>\dfrac{0,15}{2}\Rightarrow H_2SO_4\text{ dư}\\ \Rightarrow n_{BaSO_4}=n_{BaCl_2}=0,15(mol);n_{HCl}=2n_{BaCl_2}=0,3(mol)\\ n_{H_2SO_4(dư)}=0,275-0,15=0,125(mol)\\ \Rightarrow m_{BaSO_4}=0,15.233=34,95(g);m_{CT_{HCl}}=0,3.36,5=10,95\\ m_{CT_{H_2SO_4(dư)}}=0,125.98=12,25(g)\\ \Rightarrow m_{\text{dd sau p/ứ}}=180+320-34,95=465,05(g)\\ \Rightarrow \begin{cases} C\%_{H_2SO_4(dư)}=\dfrac{12,25}{465,05}.100\%=2,63\%\\ C\%_{HCl}=\dfrac{10,95}{465,05}.100\%=2,35\% \end{cases}$
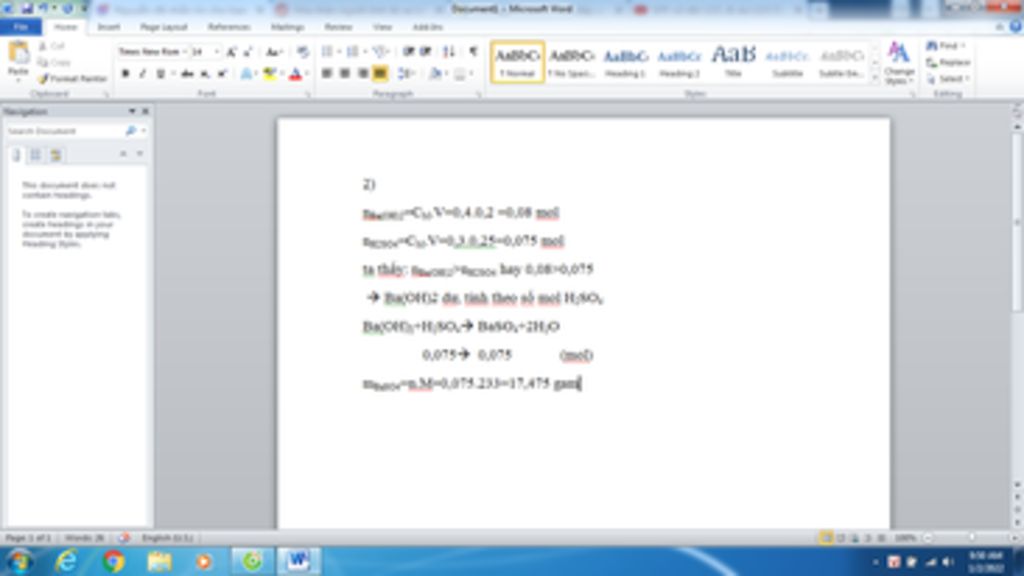
Bài 2:
$n_{Ba(OH)_2}=0,4.0,2=0,08(mol);n_{H_2SO_4}=0,3.0,25=0,075(mol)\\ PTHH:Ba(OH)_2+H_2SO_4\to BaSO_4\downarrow+2H_2O\\ \text{Lập tỉ lệ: }\dfrac{0,08}{1}>\dfrac{0,075}{1}\Rightarrow Ba(OH)_2\text{ dư}\\ \Rightarrow n_{BaSO_4}=n_{H_2SO_4}=0,075(mol)\\ \Rightarrow m_{\downarrow}=m_{BaSO_4}=0,075.233=17,475(g)$