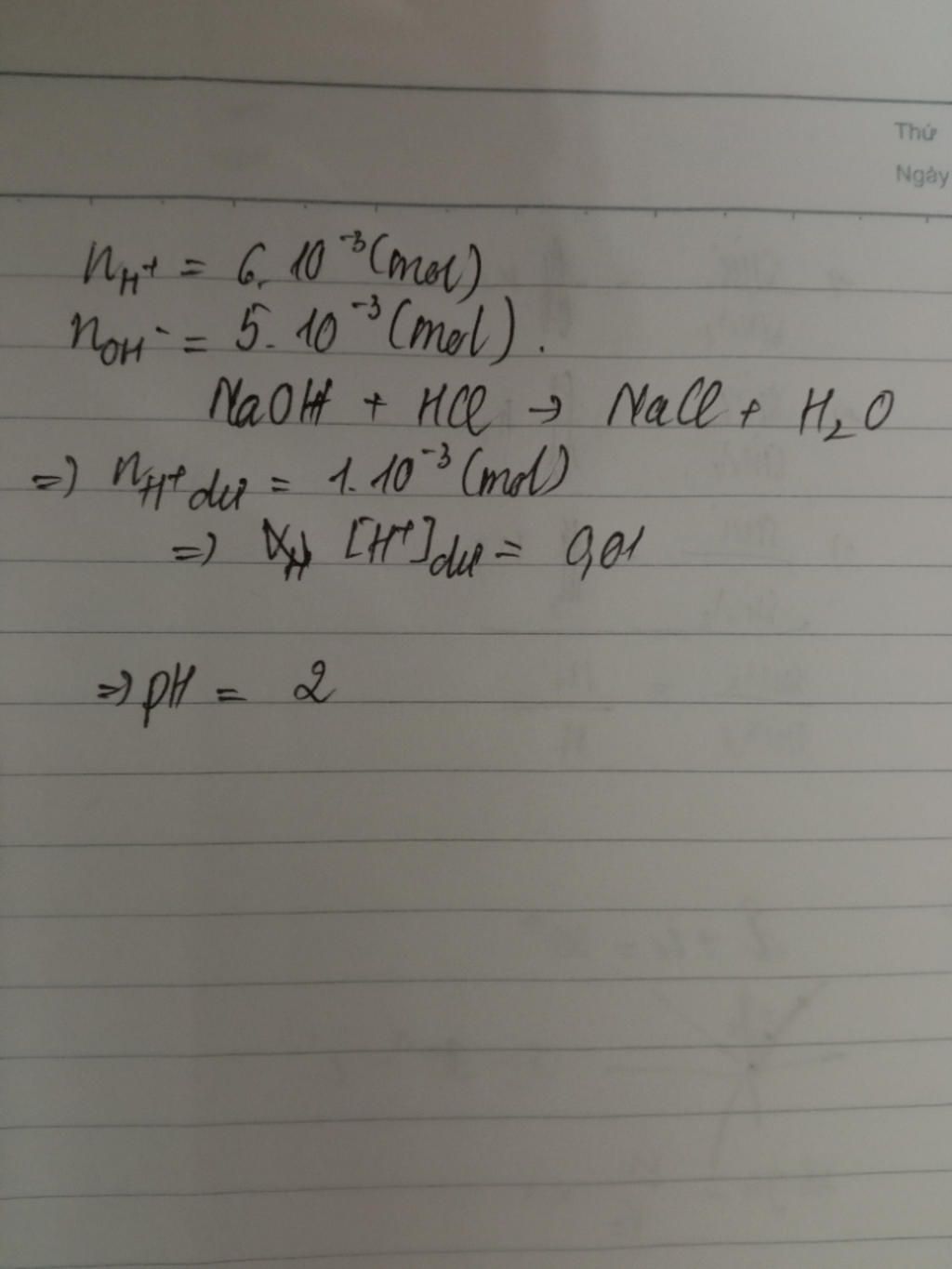Trộn lẫn 50ml dung dịch HCl 0,12M với 50ml dung dịch NaOH 0,1M . Vậy pH của dung dịch thu được bằng bao nhiêu ?
2 câu trả lời
Đáp án:
pH=2
Giải thích các bước giải:
nH+=nHCl=0,05.0,12=0,006(mol)nOH−=nNaOH=0,005(mol)H++OH−→H2OnH+>nOH−Nên H+ dư⇒nH+ dư=0,001(mol)H+=0,001:(0,05+0,05)=0,01(M)⇒pH=−log([H+])=2