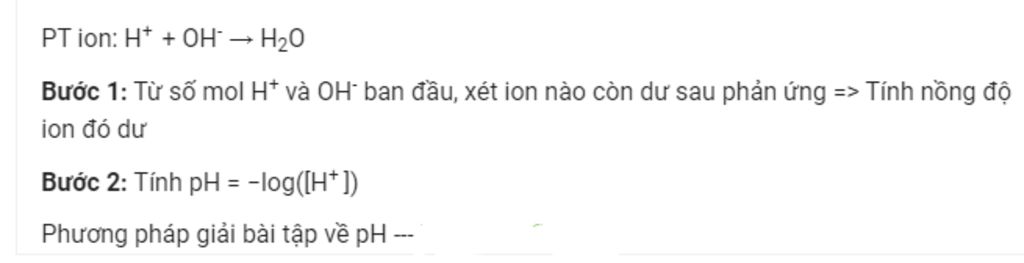
Trộn 200 ml dung dịch gồm H2SO4 0,5M và HCl 0,1M với 300 ml dung dịch gồm NaOH 0,45M và Ba(OH)2 0,15M. pH của dung dịch tạo thành là A. 2. B. 12. C. 11,7. D. Kết quả khác.
2 câu trả lời
Đáp án:
B
Giải thích các bước giải:
\(\begin{array}{l}
{n_{{H_2}S{O_4}}} = 0,5 \times 0,2 = 0,1mol\\
{n_{HCl}} = 0,2 \times 0,1 = 0,02mol\\
{n_{{H^ + }}} = 2{n_{{H_2}S{O_4}}} + {n_{HCl}} = 0,22mol\\
{n_{NaOH}} = 0,45 \times 0,3 = 0,135mol\\
{n_{Ba{{(OH)}_2}}} = 0,3 \times 0,15 = 0,045mol\\
{n_{O{H^ - }}} = {n_{NaOH}} + 2{n_{Ba{{(OH)}_2}}} = 0,225mol\\
{H^ + } + O{H^ - } \to {H_2}O\\
\dfrac{{0,22}}{1} < \dfrac{{0,225}}{1} \Rightarrow O{H^ - }\text{ dư}\\
{n_{O{H^ - }}} = 0,225 - 0,22 = 0,005mol\\
{\rm{[}}O{H^ - }{\rm{]}} = \dfrac{{0,005}}{{0,5}} = 0,01M\\
pOH = - \log (0,01) = 2\\
pH = 14 - 2 = 12
\end{array}\)
Câu hỏi trong lớp
Xem thêm