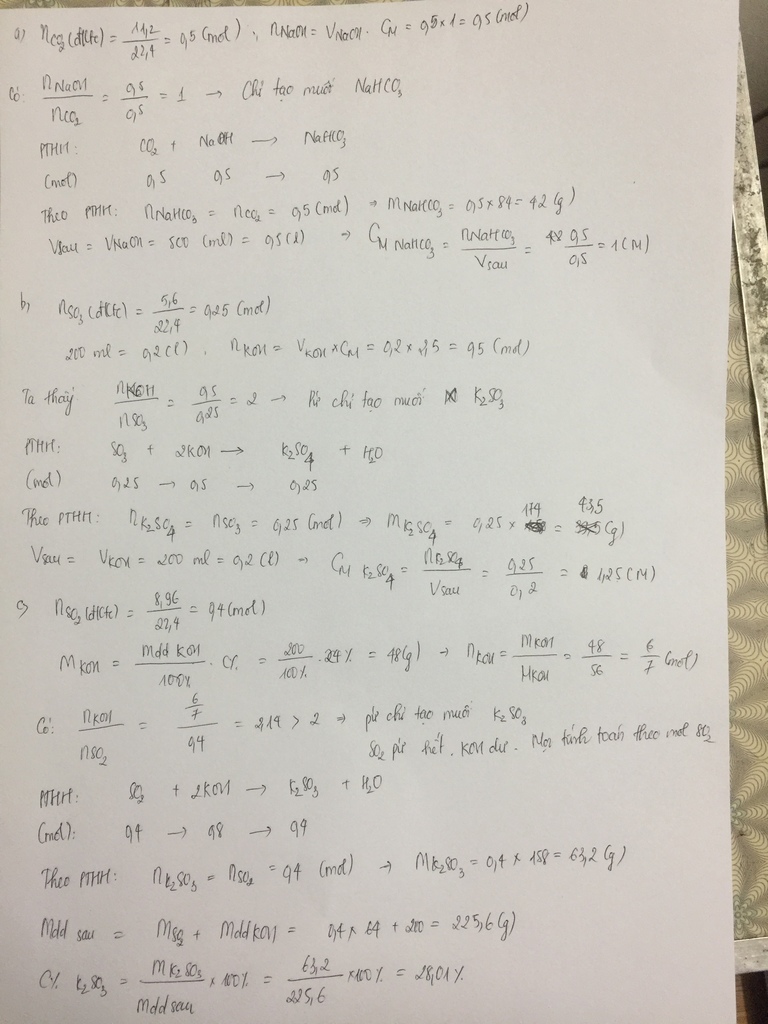Tính khối lượng muối sinh ra và nồng độ của muối trong dung dịch thu được trong các trường hợp sau: a, Cho 11,2 lít CO2 (đktc) vào bình đựng 500 ml dung dịch NaOH 1M b, Cho 5,6 lít SO3 (đktc) tác dụng với 200 ml dung dịch KOH 2,5M c, Dẫn 8,96 lít SO2 (đktc) vào 200g dung dịch KOH 24%
2 câu trả lời
Giải thích các bước giải:
a)
nCO2 = 11,2/22,4 = 0,5 mol
nNaOH = 0,5.1 = 0,5 mol
Ta thấy: \(\frac{{{n_{NaOH}}}}{{{n_{C{O_2}}}}} = \frac{{0,5}}{{0,5}} = 1\)
→ Sản phẩm thu được sau phản ứng chỉ có NaHCO3
PTHH: CO2 + NaOH → NaHCO3
0,5 0,5 0,5 (mol)
→ m muối = mNaHCO3 = 0,5.84 = 42 gam
→ CM NaHCO3 = n/V = 0,5/0,5 = 1M
b) Mình nghĩ chỗ này là SO2
nSO2 = 5,6/22,4 = 0,25 mol
nKOH = 0,2.2,5 = 0,5 mol
Ta thấy: \(\frac{{{n_{KOH}}}}{{{n_{S{O_2}}}}} = \frac{{0,5}}{{0,25}} = 2\)
→ Sản phẩm thu được sau phản ứng chỉ có K2SO3
PTHH: CO2 + 2KOH → K2SO3
0,25 0,5 → 0,25
→ m muối = mK2SO3 = 0,25.158 = 39,5 gam
→ CM K2SO3 = n/V = 0,25/0,2 = 1,25M
c)
nSO2 = 8,96/22,4 = 0,4 mol
mKOH = 200.(24/100) = 48 gam → nKOH = 48/56 ≈ 0,8571 mol
Mình nghĩ bạn chép nhầm đề câu c rồi.