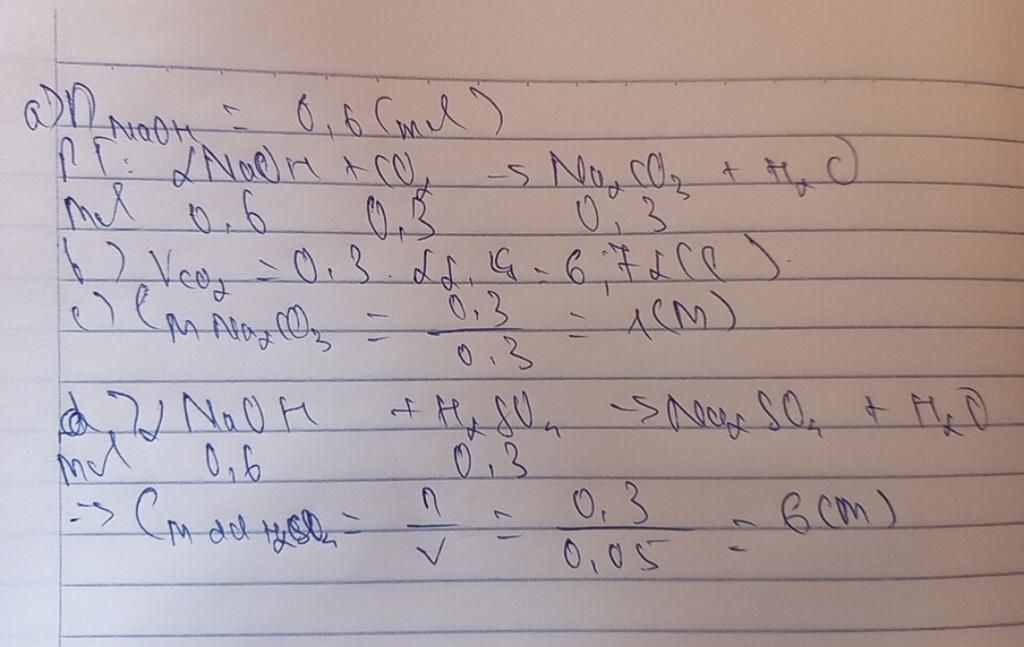Nhanhhh hộ ạ....ko phải chọn a c b d đâu nha Biết khí Co2 tác dụng vừa hết với 300 ml dung dịch NaOH 2M, sản phẩm là muối Na2Co3 và nước. a) Viết phương trình hóa học b) Tính thể tích khí Co2 đã phản ứng ở đtk (25⁰c, 1bar). c) Tính nồng độ mol/lit dung dịch muối thu được. d) Dùng 50ml dung dịch H2S04 để trung hòa hết dung dịch base NaOH trên. Tính nồng độ mol/lit dung dịch H2S04 đã dùng. ( H=1 0=16 Na=23 C=12)
2 câu trả lời
Đáp án:
\( {V_{C{O_2}}} = 7,4281{\text{ lít}}\)
\({C_{M{\text{ N}}{{\text{a}}_2}C{O_3}}} = 1M\)
\( {V_{M{\text{ }}{{\text{H}}_2}S{O_4}}} = 6M\)
Giải thích các bước giải:
Phản ứng xảy ra:
\(2NaOH + C{O_2}\xrightarrow{{}}N{a_2}C{O_3} + {H_2}O\)
Ta có:
\({n_{NaOH}} = 0,3.2 = 0,6{\text{ mol}}\)
\( \to {n_{C{O_2}}} = {n_{N{a_2}C{O_3}}} = \frac{1}{2}{n_{NaOH}} = 0,3{\text{ mol}}\)
Áp dụng công thức:
\(pV = nRT\)
Với \(p=1 \text{ bar}=0,9869 \text{ atm}\)
\(n=0,3; T=25+273=298K;R=0,082\)
\( \to {V_{C{O_2}}} = \frac{{0,3.0,082.298}}{{0,9869}} = 7,4281{\text{ lít}}\)
\({V_{dd}} = 300{\text{ ml = 0}}{\text{,3 lít}}\)
\( \to {C_{M{\text{ N}}{{\text{a}}_2}C{O_3}}} = \frac{{0,3}}{{0,3}} = 1M\)
Trung hòa axit
\(2NaOH + {H_2}S{O_4}\xrightarrow{{}}N{a_2}S{O_4} + 2{H_2}O\)
\({n_{{H_2}S{O_4}}} = \frac{1}{2}{n_{NaOH}} = 0,3{\text{ mol}}\)
\( \to {V_{M{\text{ }}{{\text{H}}_2}S{O_4}}} = \frac{{0,3}}{{0,05}} = 6M\)