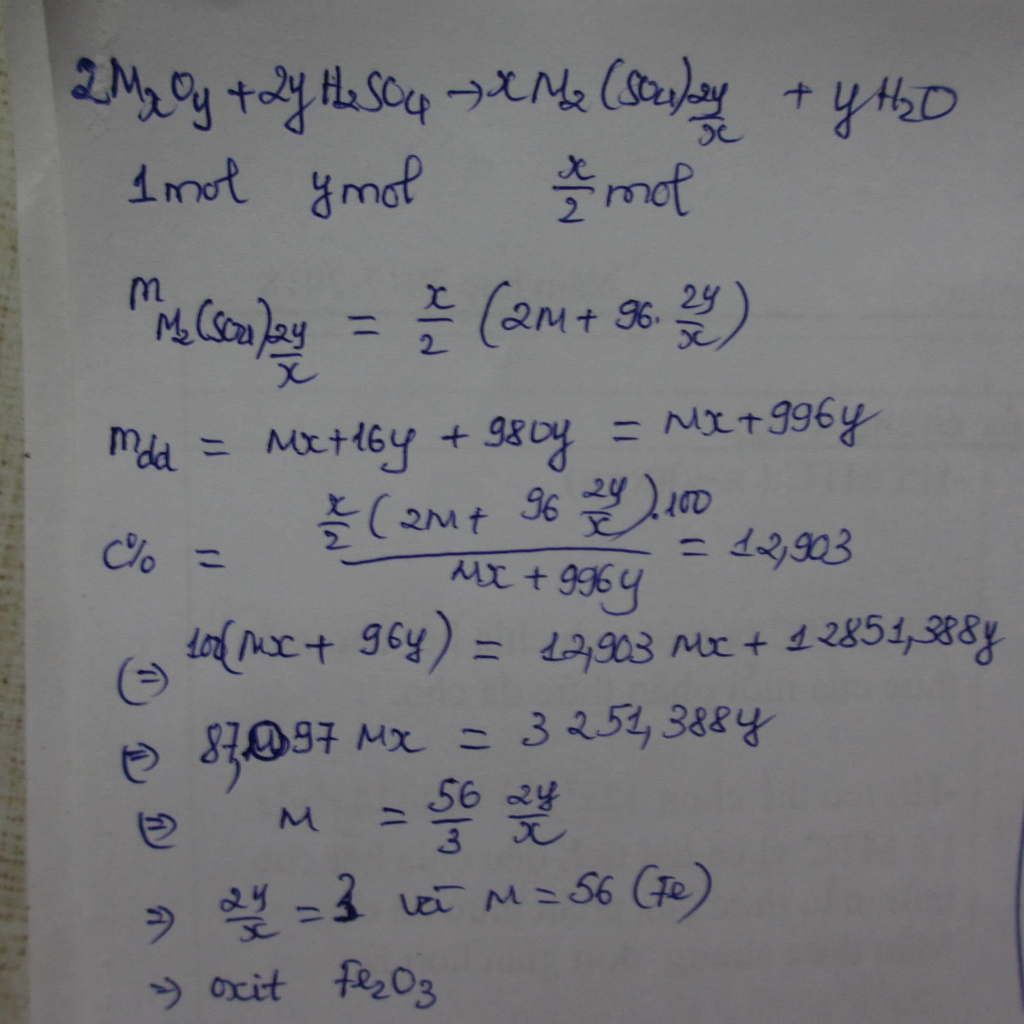hòa tan hết 3,2g oxit M2Om (M là kim loại ) trong một lượng vừa đủ dung dịch H2SO4 10% thu được dung dịch muối có nồng độ 12,9%. sau phản ứng đem cô bớt dung dịch và làm lạnh nó thu được 7,868 gam tinh thể muối với hiệu suất kết tinh là 70%. xác định công thức tinh thể muối đó giải hẳn ra hộ mình nhé mình cảm ơn
2 câu trả lời
Đáp án:
Fe2(SO4)3.9H2O
Giải thích các bước giải:
Đặt n oxit = x (mol) với x = \(\frac{{3,2}}{{2M + 16m}}\)(mol)
PTHH: M2Om + mH2SO4 → M2(SO4)m + mH2O
x → mx → x (mol)
⇒ mH2SO4 = 98mx (g) ⇒ mdd H2SO4 = 98mx.(100/10) = 980mx (g)
BTKL: m dd sau pư = 3,2 + 980mx (g)
m M2(SO4)m = x.(2M + 96m) (g)
Nồng độ muối: \(C\% = \dfrac{{x(2M + 96m)}}{{3,2 + 980mx}}.100\% = 12,9\% \)
⇒ \(\dfrac{{2M + 96m}}{{\dfrac{{3,2}}{x} + 980m}} = 0,129 \Rightarrow 2M = 30,42m + 0,4128.\dfrac{1}{x}\)
Thay x = \(\dfrac{{3,2}}{{2M + 16m}}\) vào ta được: \(2M = 30,42m + 0,4128.\dfrac{{2M + 16m}}{{3,2}}\)
$⇒ 1,742M = 32,484m ⇒ M = \dfrac{32,484m}{1,742}$
Thay m = 1, 2, 3 vào thấy m = 3; M = 56 thỏa mãn
Vậy oxit là Fe2O3.
Giả sử công thức tinh thể là Fe2(SO4)3.nH2O
BTNT Fe: n tinh thể (LT) = nFe2O3 = 3,2/160 = 0,02 mol
Do hiệu suất là 70% nên khối lượng tinh thể thu được: n tinh thể (TT) = 0,02.70% = 0,014 mol
⇒ M tinh thể = 7,868 : 0,014 = 562 (g/mol)
⇒ 400 + 18n = 562 ⇒ n = 9
Vậy công thức của tinh thể là Fe2(SO4)3.9H2O