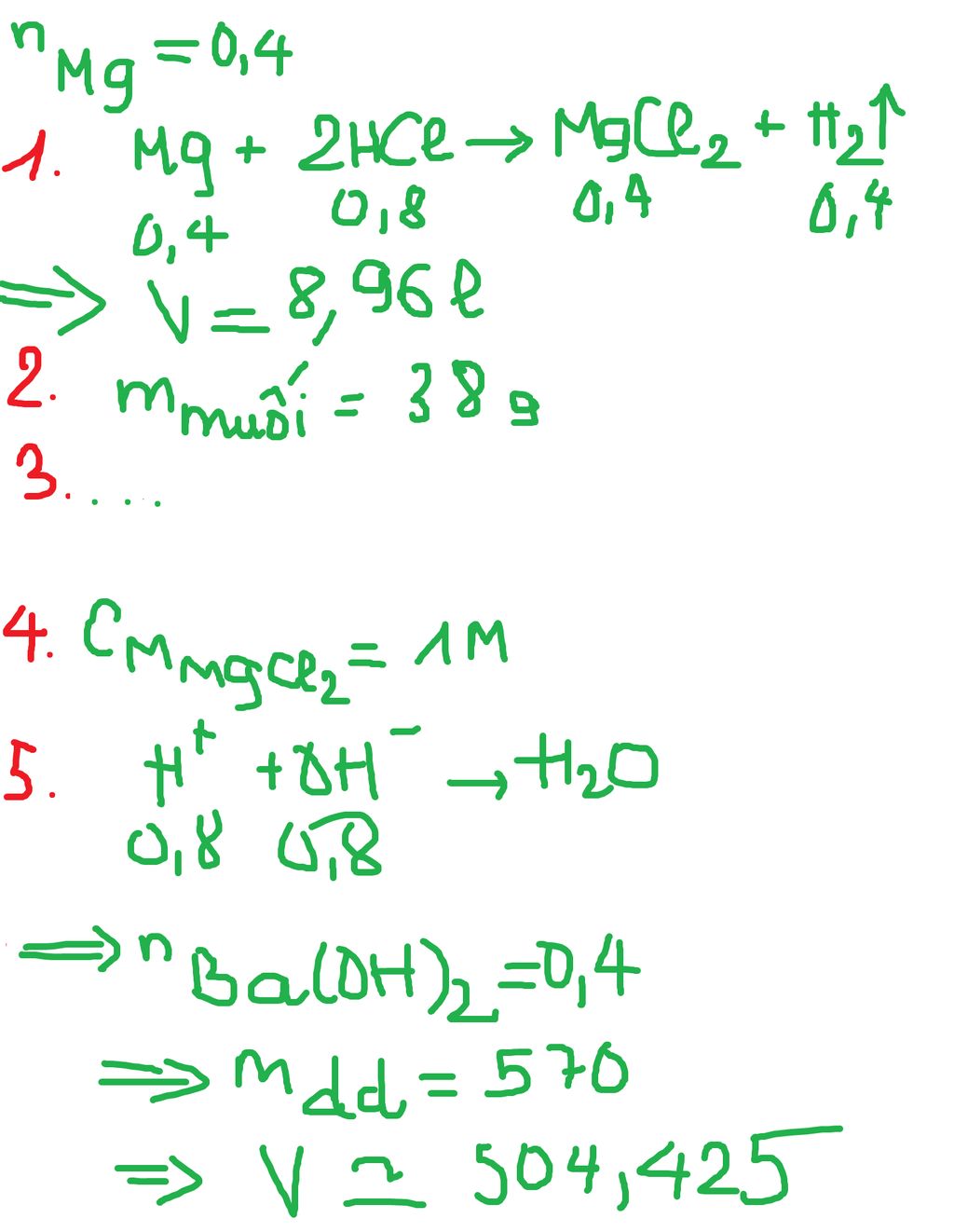Hòa tan 9,6 gam Magnesium vào 400ml dung dịch HCL loãng.Phản ứng vừa đủ 1.Tính thể tích chất khí sinh ra ở điều kiện tiêu chuẩn ? 2. Tính khối lượng muối tạo thành sau phản ứng ? 3.Tính nồng độ muối tạo thành sau phản ứng? 4..Tính nồng độ mol của chất tạo thành trong dung dịch sau phản ứng. Cho rằng thể tích của dung dịch thay đổi không đáng kể. 5.Cần bao nhiêu ml dd Ba(OH)2 12% ( D= 1,13g/ml ) để trung hòa hết lượng axit trên? Cho H= 1 O= 16 CL= 35,5 Mg = 24 nhớ viết đáp án chính thức ok (vd 1a kiểu kiểu ó )
2 câu trả lời
Đáp án:
$V_{H_2}= 8,96(l)$
$m_{MgCl_2}= 38g$
$Cm_{MgCl_2}=1M$
$Cm_{HCl}=2M$
$V_{Ba(OH)_2}=504,42ml$
Giải thích các bước giải:
$n_{Mg}=\frac{9,6}{24}= 0,4 mol$
Phương trình phản ứng:
$Mg + 2HCl \to MgCl_2 + H_2$
$Ba(OH)_2 + 2HCl \to BaCl_2 + 2H_2O$
Theo phương trình:
$n_{H_2}=n_{MgCl_2}=n_{Mg} = 0,4 mol$
$n_{HCl} =2n_{Mg}= 2.0,4=0,8 mol$
$n_{Ba(OH)_2} =\frac{1}{2}.n_{HCl}= 0,4 mol$
$V_{H_2}= 0,4.22,4= 8,96(l)$
$m_{MgCl_2}= 0,4.95=38g$
$Cm_{MgCl_2}=\frac{0,4}{0,4}=1M$
$Cm_{HCl}=\frac{0,8}{0,4}=2M$
$m_{dung dịch Ba(OH)_2}=\frac{0,4.171.100}{12}=570g$
$V_{Ba(OH)_2}=\frac{570}{1,13}=504,42ml$
Câu hỏi trong lớp
Xem thêm