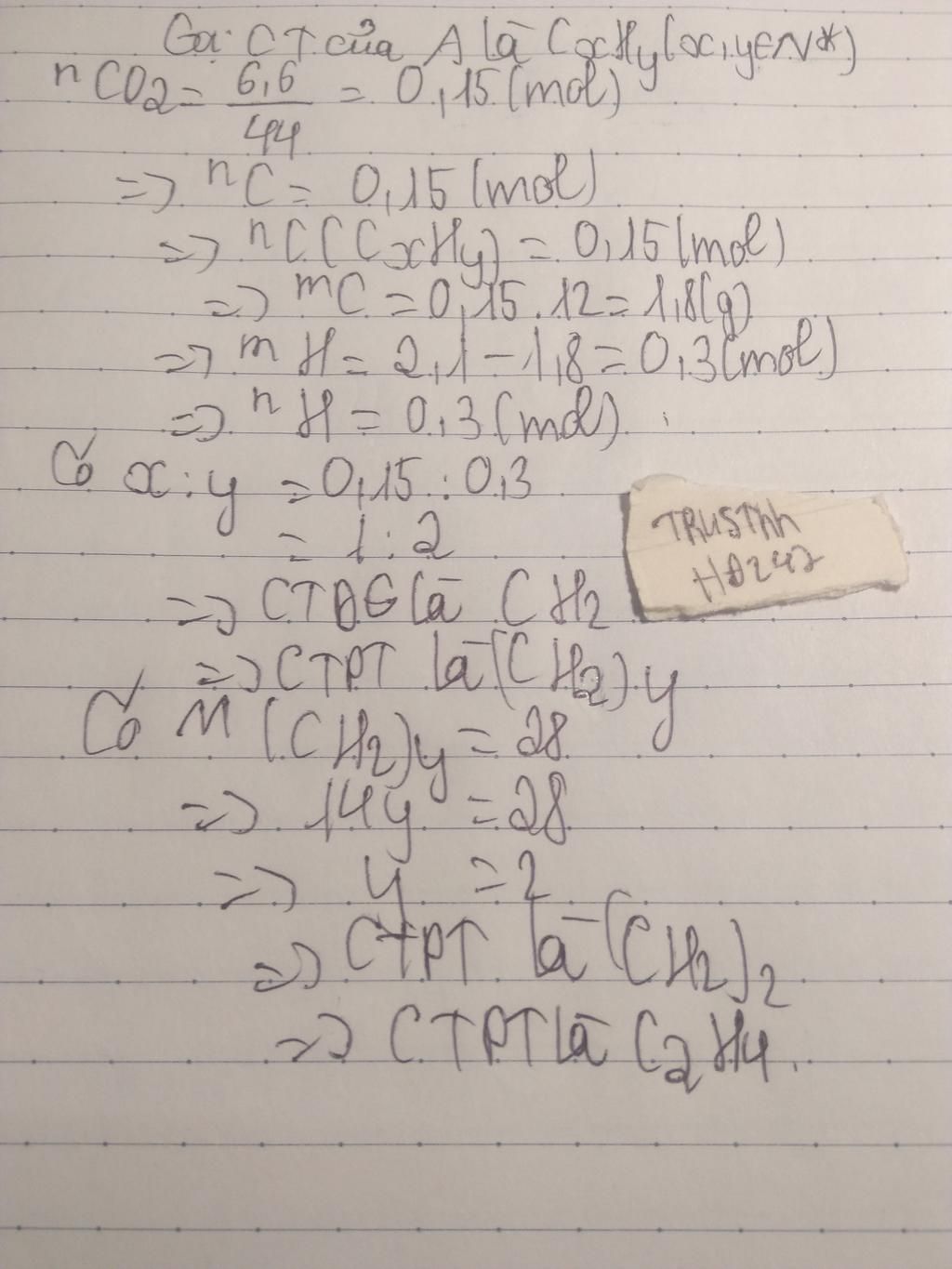đốt cháy 2,1g 1 hidrocacbon A thì thu được 6,6g CO2 tìm công thức phân tử của A biết khối lượng mol của A là 28 g/mol
2 câu trả lời
Đáp án:
$C_2H_4$
Giải thích các bước giải:
Đặt CTPT là $C_xH_y$
BTNT(C): $n_A.x=n_{CO_2}=\dfrac{6,6}{44}=0,15(mol)$
$\Rightarrow \dfrac{2,1x}{12x+y}=0,15$
$\Rightarrow 12x+y=14x$
$\Rightarrow \dfrac{x}{y}=\dfrac{1}{2}$
$\Rightarrow CTPT:(CH_2)_n$
Mà $M_A=28\Rightarrow (12+2).n=28\Rightarrow n=2$
$\Rightarrow C_2H_4$
Câu hỏi trong lớp
Xem thêm