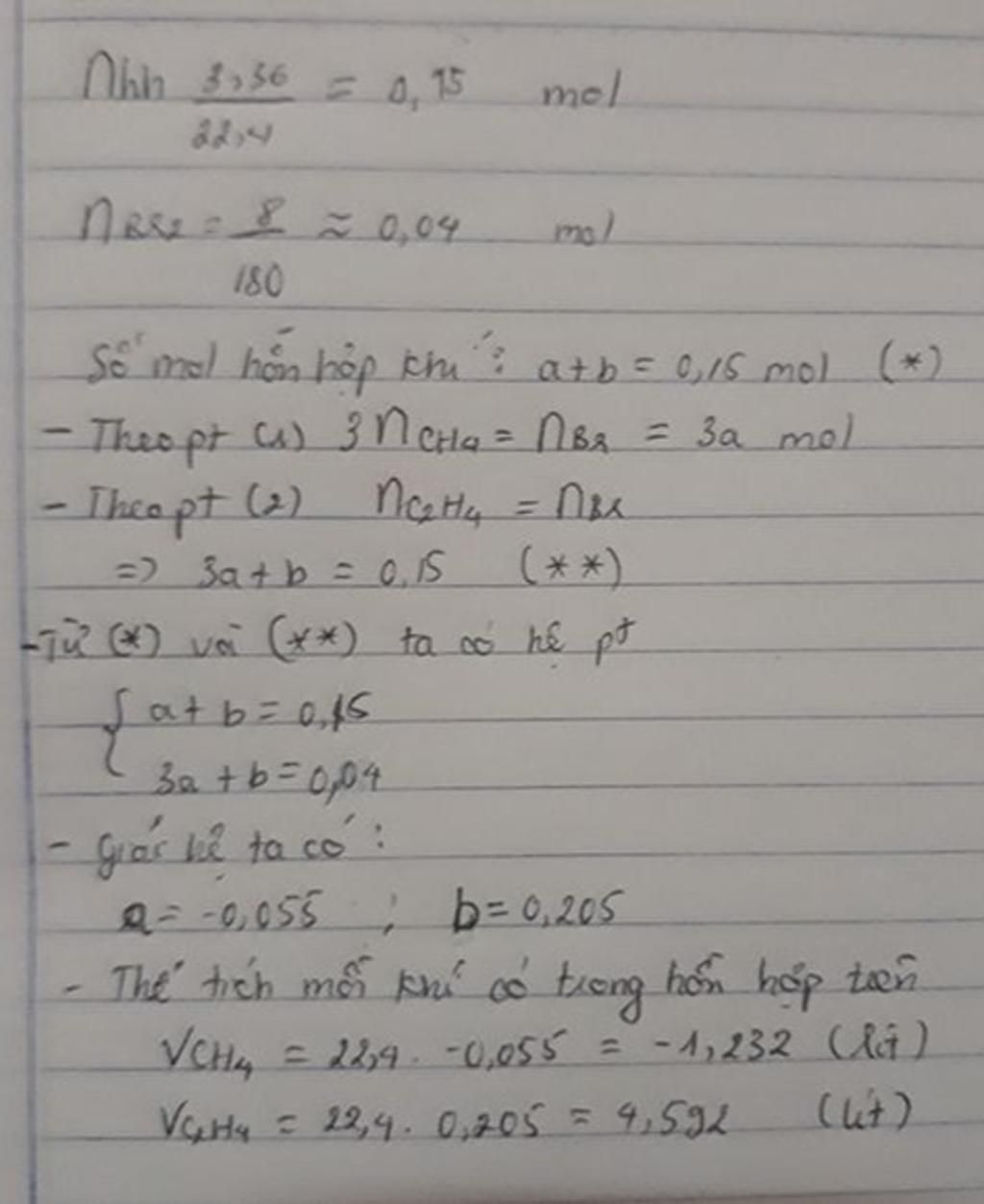Dẫn 3,36 lít hỗn hợp khí(đktc) gồm CH4 và C2H4 lội qua dung dịch Brom dư. Sau phản ứng thấy có 8 gam dung dịch Brom đã phản ứng
a/Viết phương trình phản ứng xảy ra
b/Tính thể tích mỗi khí có trong hỗn hợp trên
2 câu trả lời
Đáp án:
$ V_{C_2H_4}=1,12(l)$
$ V_{CH_4}=2,24(l)$
Giải thích các bước giải:
$a)$ $CH_4$ không phản ứng $Brom$
Phản ứng xảy ra.
$C_2H_4+Br_2\to C_2H_4Br_2$
$b)$
$n_{hh\ khí}=\dfrac{3,36}{22,4}=0,15\ (mol)$
$n_{Br_2}=\dfrac{8}{160}=0,05\ (mol)=n_{C_2H_4}$
$\to V_{C_2H_4}=0,05.22,4=1,12(l)$
$\to V_{CH_4}=3,36-1,12=2,24(l)$
Câu hỏi trong lớp
Xem thêm