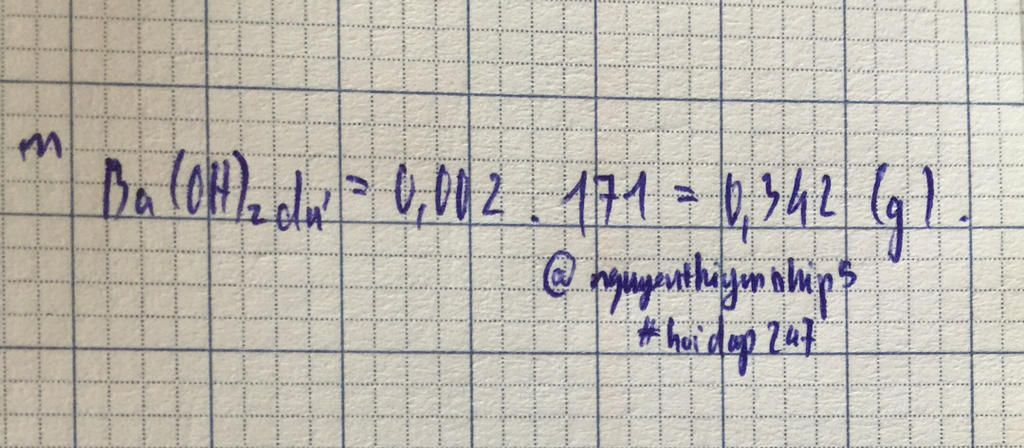Dẫn 112ml khí CO2 (đktc) đi qua 700 ml dung dịch Ba(OH)2 có CM=0.01(M)
A, viết pthh
B, tính khối lượng các chất sau phản ứng.
2 câu trả lời
Đáp án:
$a)CO_2+Ba(OH)_2\to BaCO_3\downarrow+H_2O$
$b)m_{Ba(OH)_2(dư)}=0,342(g)$
$m_{BaCO_3}=0,985(g)$
Giải thích các bước giải:
$a)$ Đổi $112ml=0,112l$ và $700ml=0,7l$
$\Rightarrow n_{CO_2}=0,005(mol);n_{Ba(OH)_2}=0,007(mol)$
$\Rightarrow n_{OH^-}=2n_{Ba(OH)_2}=0,014(mol)$
$\Rightarrow T=\dfrac{0,014}{0,005}=2,8>2$
$\Rightarrow $ Tạo muối trung hòa
$PTHH:CO_2+Ba(OH)_2\to BaCO_3\downarrow+H_2O$
$b)$ Xét tỉ lệ: $n_{CO_2}<n_{Ba(OH)_2}\Rightarrow Ba(OH)_2$ dư
$\to$ Sau p/ứ có $Ba(OH)_2$ dư và $BaCO_3$
Theo PT: $n_{Ba(OH)_2}=n_{BaCO_3}=0,005(mol)$
$\Rightarrow n_{Ba(OH)_2(dư)}=0,007-0,005=0,002$
$\Rightarrow m_{Ba(OH)_2(dư)}=0,002.171=0,342(g)$
$m_{BaCO_3}=0,005.197=0,985(g)$