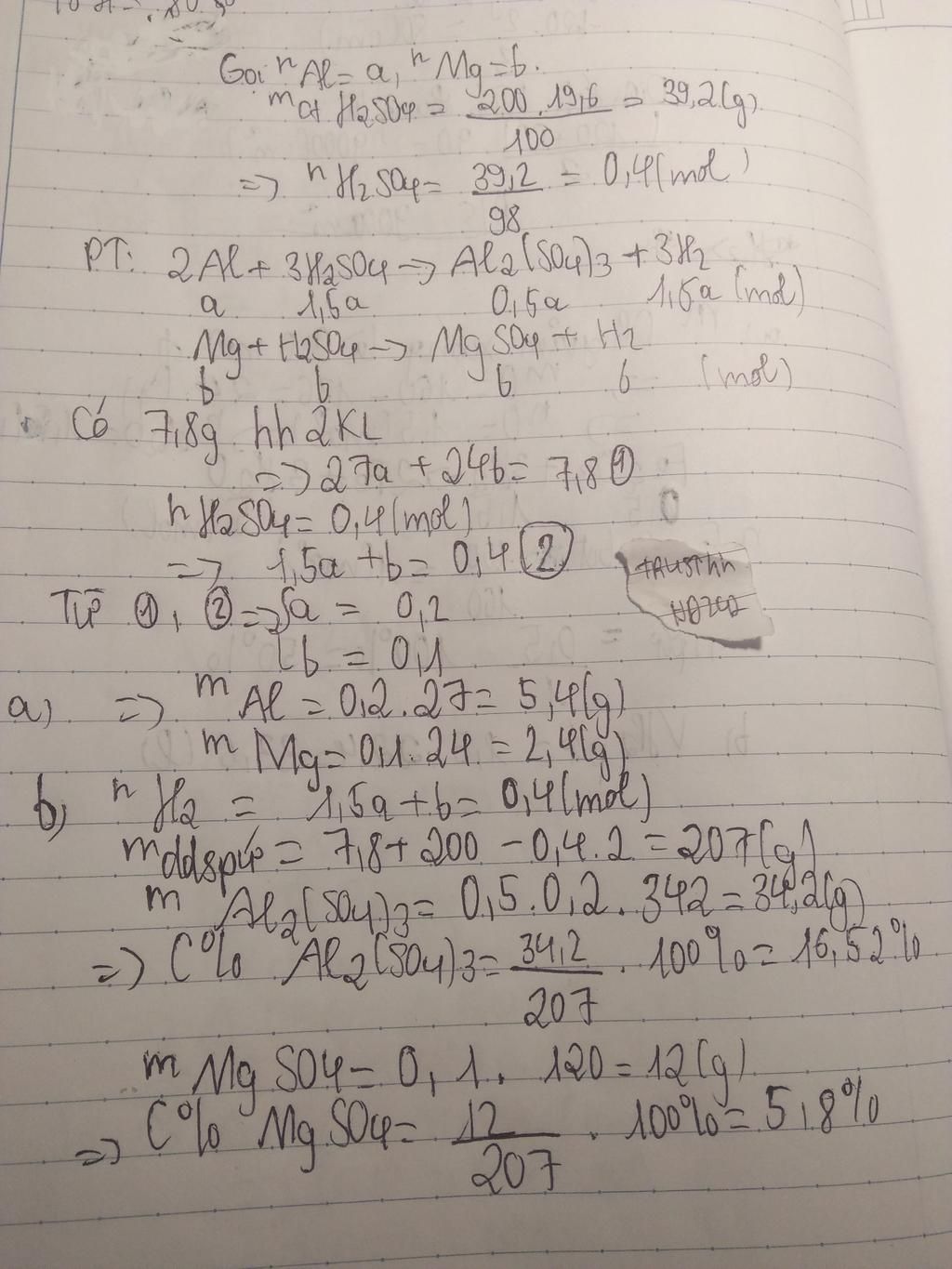Cho 7,8 g hỗn hợp hai kim loại Al và Mg, tác dụng vừa đủ với 200g dung dịch H2SO4 19,6% a) Tính khối lượng mỗi kim loại trong hỗn hợp b)Tính nồng độ phần trăm của các dung dịch sau phản ứng
2 câu trả lời
Đáp án:
`a.`
`m_{Mg} = 2,4g`
`m_{Al} = 5,4g`
`b.`
`C%_{MgSO_4} = 5,8%`
`C%_{Al_2 (SO_4)_3} = 16,52%`
Giải thích các bước giải:
`m_{H_2 SO_4} = (200 . 19,6)/100 = 39,2 (g)`
`-> n_{H_2 SO_4} = (39,2)/98 = 0,4 (mol)`
`Mg + H_2 SO_4 -> MgSO_4 + H_2↑`
`x` `x` `x` `x`
`2Al + 3H_2 SO_4 -> Al_2 (SO_4)_3 + 3H_2↑`
`y` `1,5y` `0,5y` `1,5y`
Gọi `x, y` lần lượt là số mol của `Mg, Al`
`a.`
Ta có hệ phương trình: $\begin{cases} 24x+27y=7,8\\x+1,5y=0,4\\\end{cases}$ `->` $\begin{cases} x=0,1\\y=0,2\\\end{cases}$
`m_{Mg} = 0,1 . 24 = 2,4 (g)`
`m_{Al} = 7,8 - 2,4 = 5,4 (g)`
`b.`
`n_{H_2} = 0,1 + 1,5 . 0,2 = 0,4 (mol)`
`-> m_{H_2} = 0,4 . 2 = 0,8 (g)`
`m_{ddsaupu} = m_{hh} + m_{ddH_2 SO_4} - m_{H_2}`
`-> m_{ddsaupu} = 7,8 + 200 - 0,8 = 207 (g)`
Các dung dịch thu được sau phản ứng là `MgSO_4` và `Al_2 (SO_4)_3`
`m_{MgSO_4} = 0,1 . (24 + 32 + 16 . 4) = 12 (g)`
`-> C%_{MgSO_4} = (12 . 100)/207 = 5,8 (%)`
`m_{Al_2 (SO_4)_3} = 0,5 . 0,2 . (27 . 2 + 32 . 3 + 16 . 12) = 34,2 (g)`
`-> C%_{Al_2 (SO_4)_3} = (34,2 . 100)/207 = 16,52 (%)`