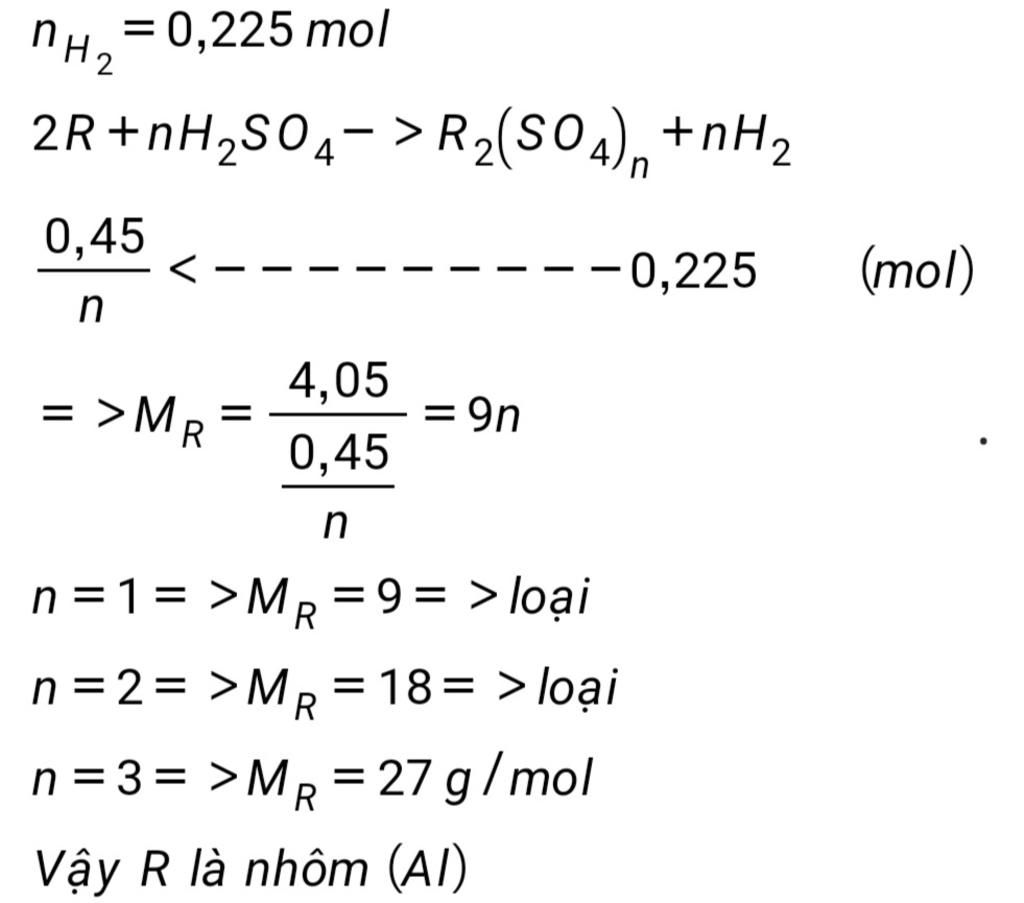Cho 4,05 gam một kim loại R tác dụng với dung dịch axit H2SO4 loãng , dư sau phản ứng thu được 5,04 lít khí ở điều kiện chuẩn. R là kim loại nào
2 câu trả lời
Đáp án:
Giải thích các bước giải:
Gọi `m` là hóa trị của `R`
PTHH: `2R + mH_2 SO_4 -> R_2 (SO_4)_m + mH_2`
`nH_2 = (5,04)/(22,4) = 0,225 (mol)`
Theo PT: `nR = nH_2 . 2/m = (0,45)/m`
`-> `M_R = (4,05)/((0,45)/m)` $(g/mol)$
Kim loại có 3 hóa trị nên ta có bảng:
$\left[\begin{array}{ccc}m&1&2&3\\M_R&9&18&27\\&loại&loại&lấy\end{array}\right]$
`-> R` là `Al` (nhôm)
Câu hỏi trong lớp
Xem thêm