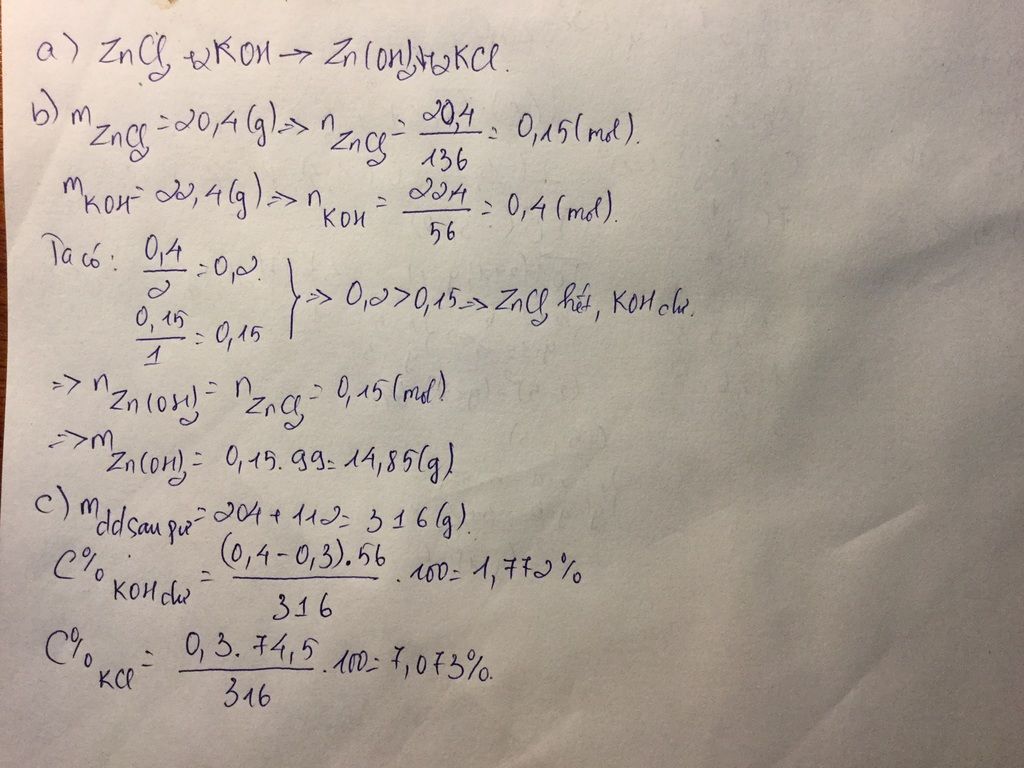Cho 204g dd muối ZnCl 10% tác dụng với 112g dd KOH 20% a) viết phương trình hoá học b) tính khối lượng kết tủa thu được c) tính nồng độ phần trăm của chất thu được sau phản ứng
2 câu trả lời
Đáp án:
b) 14,85 gam
c)
%K2ZnO2=2,9%
%KCl=7,42%
Giải thích các bước giải:
a)
ZnCl2 + 2KOH -> Zn(OH)2 + 2KCl
Ta có: mZnCl2=204.10%=20,4 gam -> nZnCl2=20,4/(65+35,5.2)=0,15 mol.
mKOH=112.20%=22,4 gam -> nKOH=22,4.(39+17)=0,4 mol
Ta có: nKOH > 2nZnCl2 -> KOH dư ở phản ứng đầu.
Phản ứng này ZnCl2 phản ứng hết 0,15 mol -> KOH phản ứng 0,3 mol thu được 0,15 mol Zn(OH)2.
Còn dư lại 0,1 mol KOH.
Zn(OH)2 + 2KOH -> K2ZnO2 + 2H2O
Ta có: nZn(OH)2=0,2 mol; nKOH=0,1 mol -> Zn(OH)2 dư
-> nZn(OH)2 phản ứng=0,1/2=0,05 mol
Sau phản ứng kết tủa là Zn(OH)2 0,2-0,05=0,15 mol -> mZn(OH)2=14,85 gam
BTKL: m dung dịch sau phản ứng=204+112 -mZn(OH)2=301,15 gam
Dung dịch sau phản ứng chứa K2ZnO2 0,05 mol và KCl 0,3 mol
-> mK2ZnO2=8,75 gam -> %K2ZnO2=2,9%
mKCl=22,35 gam -> %KCl=7,42%
Câu hỏi trong lớp
Xem thêm