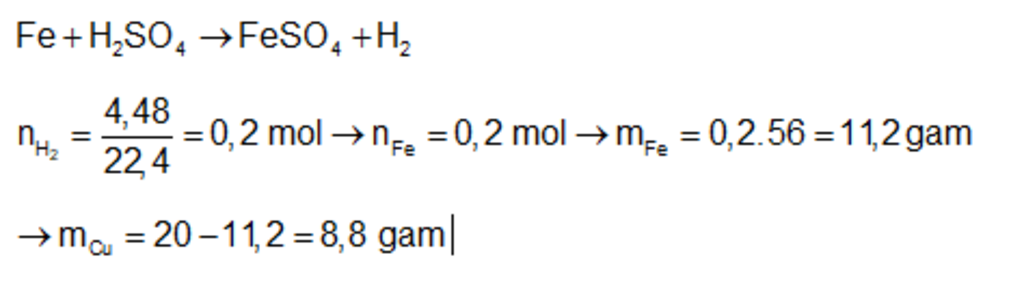Cho 20 gam 2 KL đồng và sắt t/d với H2SO4 loãng dư thu dc 4,48l khí hidro. Tính khối lg từng kl trong hỗn hợp ban đầu
2 câu trả lời
Đáp án: $m_{Fe}$ = $11,2(g)_{}$ ; $m_{Cu}$ = $8,8(g)_{}$
Giải thích các bước giải:
$Cu + H_{2}$$SO_{4}$ --x-->
$Fe_{}$ + $H_{2}$$SO_{4}$ → $FeSO_{4}$ + $H_{2}$ ↑
1 1 1 1 (mol)
0,2 0,2 0,2 0,2 (mol)
Tóm tắt:
$m_{hh}$ = $m_{Cu}$ + $m_{Fe}$ = $20(g)_{}$
$VH_{2}$ = $4,48(l)_{}$ (Bạn xem lại đề nha khí này phải ở điều kiện tiêu chuẩn lúc đó mới tính số mol được)
Tính số mol: $nH_{2}$ = $\frac{VH_2}{22,4}$ = $\frac{4,48}{22,4}$ = $0,2(mol)_{}$
Tính theo yêu cầu:
$m_{Fe}$ = $n_{Fe}$ * $M_{Fe}$
= $0,2 * 56_{}$
= $11,2(g)_{}$
$m_{Cu}$ = $m_{hh}$ - $m_{Fe}$
= $20 - 11,2_{}$
= $8,8(g)_{}$
(Chỗ n, V $H_{2}$ bạn ghi $H_{2}$ dưới mấy chữ đó giùm mình nha)