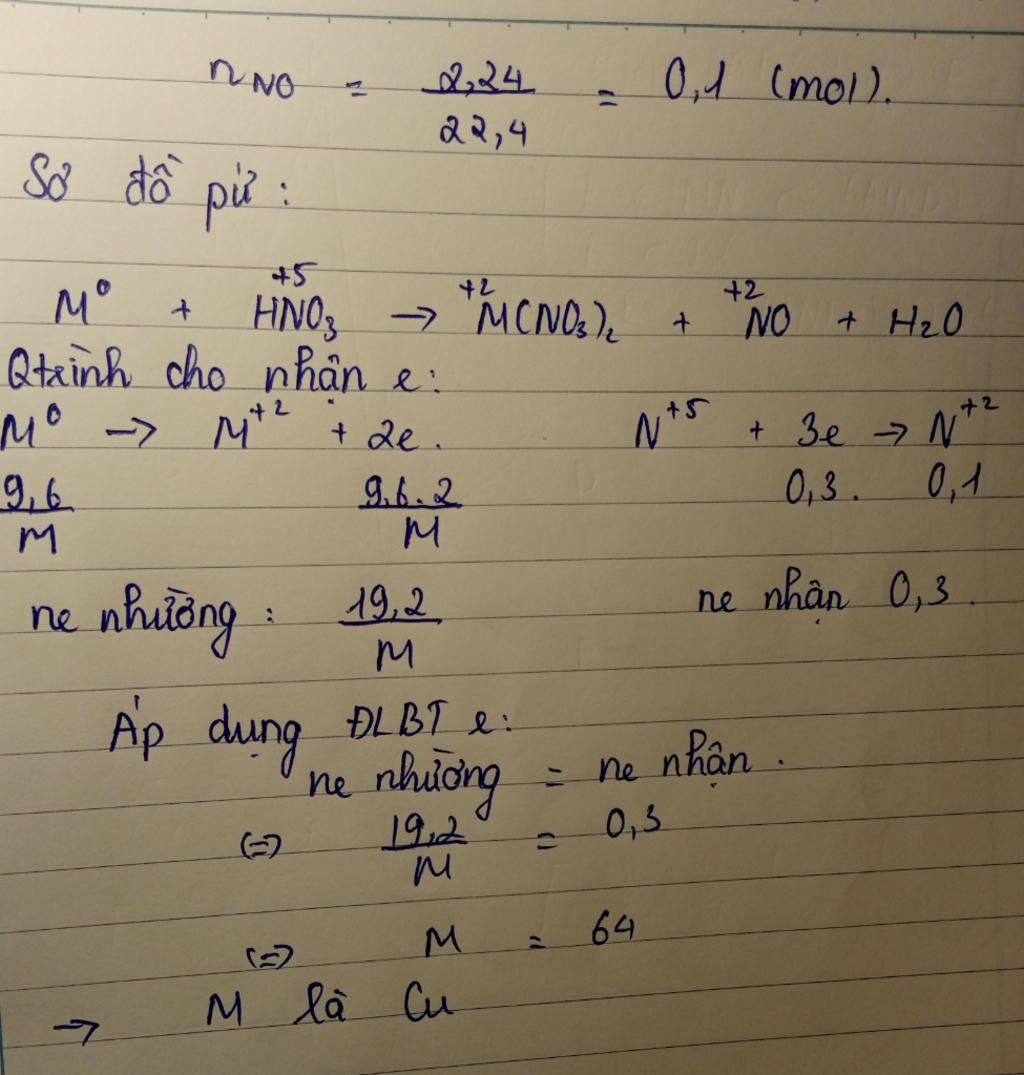Bài 1: Cho 9,6 gam một kim loại M (có hóa trị II) tác dụng hết với dung dịch HNO3 loãng dư. Sau phản ứng thu được 2,24 lít khí NO (sản phẩm khử duy nhất, đo ở đktc). Xác định tên kim loại M?
2 câu trả lời
`-` `n_{NO} = \frac{2,24}{22,4} = 0,1` `(mol)`
Phương trình hóa học: `M^o + HNO_3 -> M(NO_3)_2 + NO\uparrow + H_2O`
Theo phương trình `n_{M} = \frac{9,6}{M}`
Quá trình cho `e`: `M^o -> M^{+2} + 2e`
`->` `\frac{9,6}{M} -> \frac{19,2}{M} -> e` nhường: `\frac{19,2}{M}`.
Quá trình nhận `e`: `N^{+5} + 3e -> N^{+2}`
`->` `0,3 -> 0,1 -> e` nhận: `0,3`.
Áp dụng định luật bảo toàn electron, ta có:
`e` cho `= e` nhận
`<=>` `\frac{19,2}{M} = 0,1`
`<=>` `M = 64`
`->` `M` là nguyên tố Đồng `(Cu)`.
$#BROTHERS$