Nung m gam hỗn hợp gồm Mg và Cu(NO3)2 trong điều kiện không có không khí, sau một thời gian thu được rắn X và 6,384 lít (đktc) hỗn hợp khí Y. Hòa tan hoàn toàn X bằng 500 ml; dung dịch HCl 2M, thu được dung dịch Z chỉ chứa 54,42 gam muối và 0,05 mol hỗn hợp khí T gồm hai khí trong đó có N2. Tỉ khối của T so với He bằng 5,7.
Cho các phát biểu sau:
(a) Giá trị của m là 39,64.
(b) Trong Y có chứa 0,045 mol O2.
(c) Nếu tiếp tục nung X đến khối lượng không đổi thì thu được 2 chất rắn.
(d) Dung dịch Z chỉ chứa 1 anion.
(e) Dung dịch Z chứa 2 cation.(d) Số phát biểu đúng là:
Trả lời bởi giáo viên
Bước 1: Viết sơ đồ tóm tắt đề bài
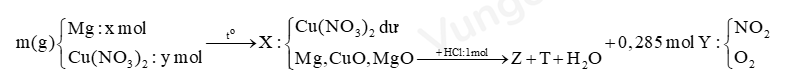
Bước 2: Xác định thành phần của Z, tính số mol các chất trong Z- 54,42 gam Z: Mg2+ x (mol) ; Cu2+ y (mol) ; Cl- 1 (mol) ; NH4+ z (mol).
- Lập hệ phương trình tính x, y, z:
+ mmuối = 24x + 4y + 18z + 1.35,5 = 54, 42
+ BTĐT: 2x + 2y + z = 1
+ BTNT O: nH2O = y - 0,285.2 = y - 0,57
+ 0,05 mol T: N2 0,04 mol ; H2 0,01 mol (dựa vào tỉ khối so với He $\overline M $= 22,8, áp dụng sơ đồ đường chéo tính nN2, nH2).
BTNT H: 2(y - 0,57) + 4z + 0,01.2 = 1
⟹ x = 0,32 ; y = 0,17 ; z = 0,02
Bước 3: Xét các phát biểu, xác định phát biểu đúng(a) Đúng, m = mMg + mCu(NO3)2 = 39,4 g
(b) Đúng
BTNT N ⟹ nNO2 = 2y - x - 2nN2 = 0,24 mol
⟹ nO2 = nY - nNO2 = 0,045 mol
(c) Sai
Thu được 3 chất rắn MgO, Cu, CuO dư:
PTHH: Mg + Cu(NO3)2 → CuO + MgO + 2NO2
nCu(NO3)2 = 0,17 mol ⟹ nMg = nCuO = nMgO = 0,17 mol
Mg + CuO → MgO + Cu
nMg = 0,32 - 0,17 = 0,15 mol ⟹ nCuO = nMgO = 0,15 mol
⟹ nCuO dư = 0,02 mol
(d) Đúng, do có chứa H2 nên NO3- hết, Z chỉ chứa 1 anion là Cl-
(e) Sai, Z chứa 3 cation Mg2+, Cu2+, NH4+
- Vậy có 3 phát biểu đúng
Hướng dẫn giải:
Bước 1: Viết sơ đồ tóm tắt đề bài
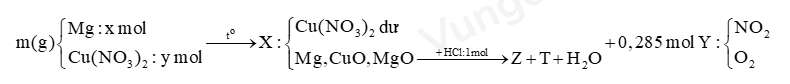
Bước 2: Xác định thành phân của Z, tính số mol các chất trong Z
- Xác định các ion có trong Z.
- Lập hệ phương trình tính số mol các chất:
+ Dựa vào tổng mmuối
+ BTĐT
+ BTNT O và H.
Bước 3: Xét các phát biểu, xác định phát biểu đúng