tổng số các loại hạt cơ bản trong nguyên tử nguyên tố X là 36 hạt, trong đó số hạt không mang điện chiếm 33,33%. a) tìm số hạt mỗi loại và vẽ sơ đồ cấu tạo nguyên tử của nguyên tố X b) - X là ng.tố nào ( tên, KHHH ) ? - Xác định vị trí của X trong bảng tuần hoàn ( số thứ tự ô, chu kì, nhóm ) c) so sánh tính kim loại của ng.tố X với các nguyên tố lân cận ? GIÚP E VỚI Ạ, EM CẦN GẤP LẮM. EM CẢM ƠN ANH CHỊ NHIỀU LẮM !!! ( 30' NỮA EM NỘP RỒI Ạ )
1 câu trả lời
Giải thích các bước giải:
a/.
Tổng số các loại hạt cơ bản trong nguyên tử nguyên tố X là 36 hạt
⇔ $p+e+n=36$
Mà $p=e$
⇒ $2p+n=36$
Số hạt không mang điện ($n$) chiếm 33,33%.
⇔ $n=$ `(33,33%.36)/(100%)` $=12 hạt$
⇒ $2p+n=36$
⇔ $2p+12=36$
⇒ $p=$ `(36-12)/2` $=12$
Vậy $p=e=12$; $n=12$
⇒ $Z=p=e=12$
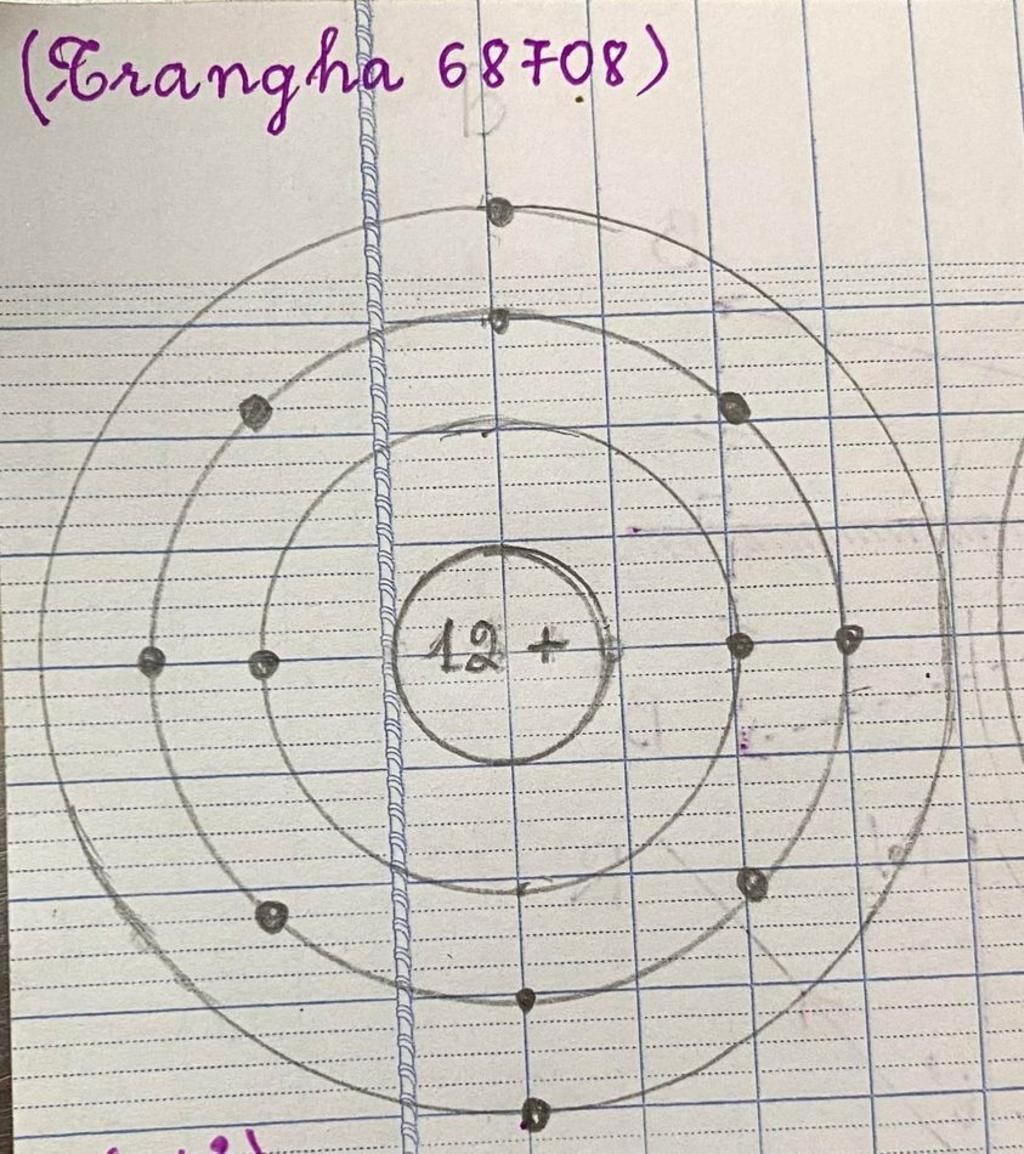
Vẽ sơ đồ cấu tạo nguyên tử của nguyên tố X: Xem hình
b/.
$X$ là nguyên tố $Magie$ $KHHH:Mg$
+ $Mg(Z=12)$ nằm ở ô thứ $12$ trong bảng tuần hoàn
+ $Mg$ có 3 lớp electron nên thuộc chu kỳ $3$ trong bảng tuần hoàn.
+ $Mg$ có $2e$ lớp ngoài cùng, nên thuộc nhóm $IIA$.
c/.
$Mg$ thuộc nhóm kim loại kiềm thổ
Trong chu kỳ $3$, tính kim loại của $Mg$ so với các kim loại lân cận là:
$Mg<Na$
$Mg>Al$
Xếp theo tính kim loại giảm dần: $Na>Mg>Al$