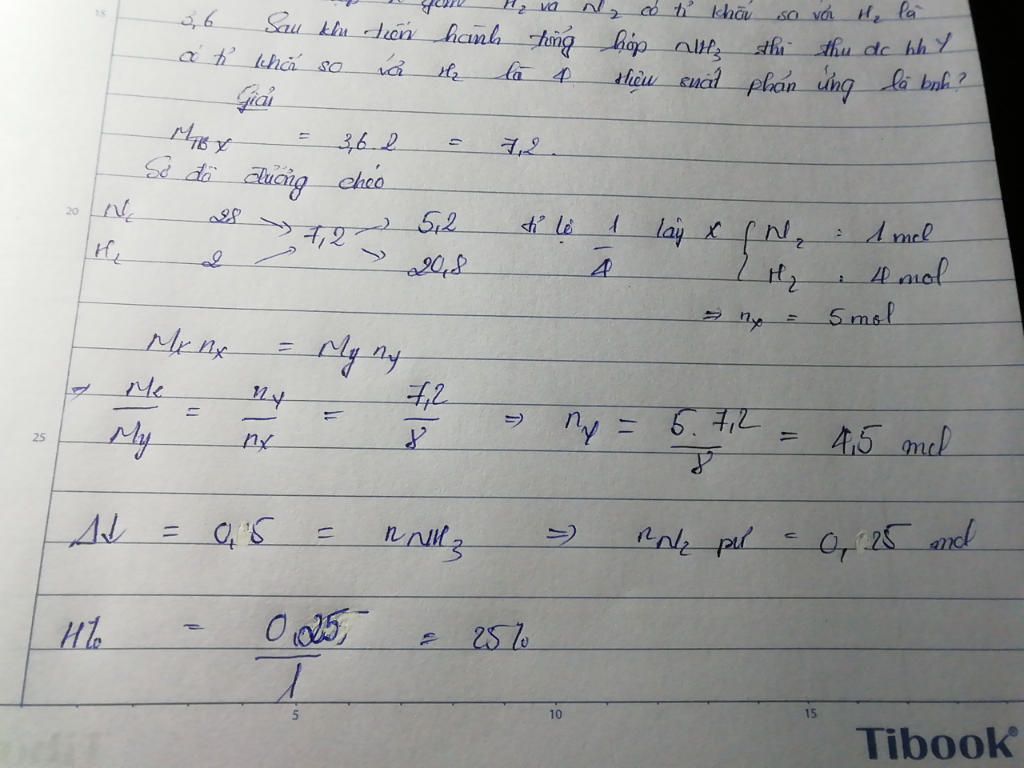hỗn hợp X gồm có H2 và N2 có tỉ khối so với Hidro là 3,6 sau khi tiến hành phản ứng tổng hợp NH3 thu được hỗn hợp Y có tỉ khối hơi so với Hidro là 4 hiệu suất của phản ứng tổng hợp là
2 câu trả lời
Đáp án:
$25\% $
Giải thích các bước giải:
Ta có:
\(\overline {{M_X}} = 3,6{M_{{H_2}}} = 3,6.2 = 7,2\)
Áp dụng quy tắc đường chéo:
\(\begin{array}{*{20}{c}}
{{N_2}(28)}&{}&{5,2} \\
{}&{X(7,2)}&{} \\
{{H_2}(2)}&{}&{20,8}
\end{array} \to \dfrac{{{n_{{N_2}}}}}{{{n_{{H_2}}}}} = \dfrac{{5,2}}{{20,8}} = \dfrac{1}{4}\)
Giả sử hỗn hợp ban đầu có 1 mol \(N_2\) và 4 mol \(H_2\)
Phản ứng xảy ra:
\({N_2} + 3{H_2}\xrightarrow{{{t^o},xt}}2N{H_3}\)
Vì \({n_{{H_2}}} > 3{n_{{N_2}}}\) nên \(H_2\) dư so với \(N_2\)
Gọi số mol \(N_2\) phản ứng là \(x\) suy ra \(H_2\) phản ứng là \(3x\)
Sau phản ứng
\({n_{{N_2}}} = 1 - x;{n_{{H_2}}} = 4 - 3x;{n_{N{H_3}}} = 2x\)
\( \to {n_Y} = 1 - x + 4 - 3x + 2x = 5 - 2x\)
\({m_Y} = {m_X} = 1.28 + 4.2 = 36\)
\( \to \overline {{M_Y}} = \dfrac{{36}}{{5 - 2x}} = 4{M_{{H_2}}} = 4.2 = 8\)
\( \to x=0,25\)
Hiệu suất phản ứng:
\(H = \dfrac{{0,25}}{1} = 25\% \)