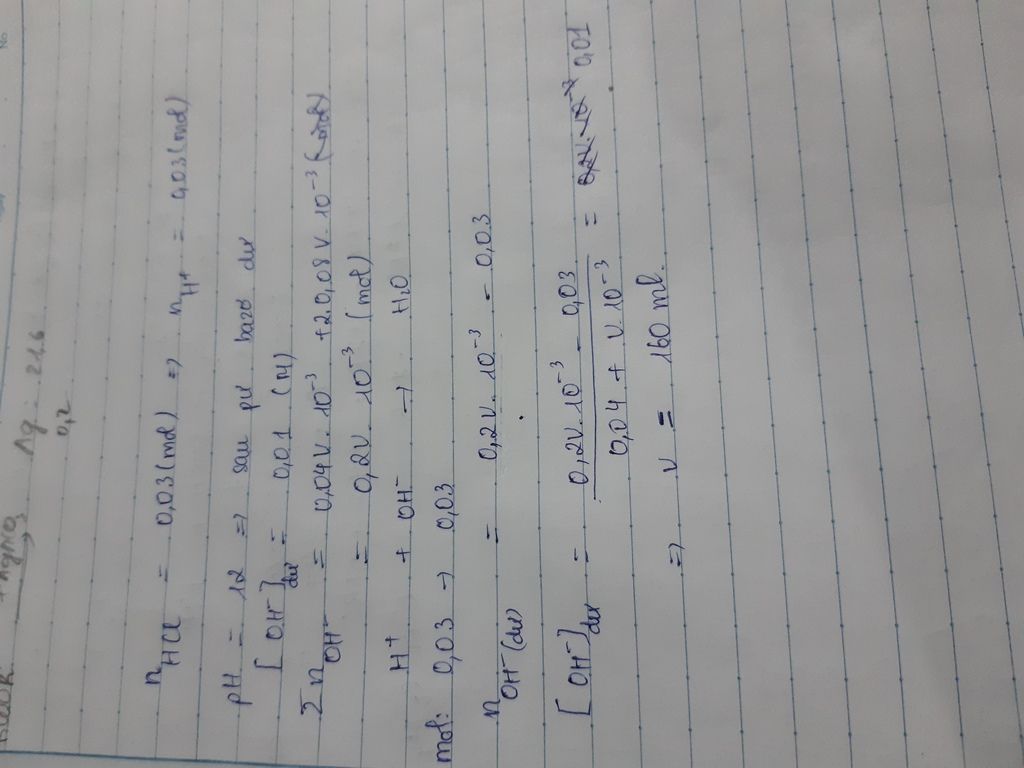cho 40ml dd hcl 0,75 M vào V ml dd chứa đồng thời KOH 0,04m VÀ ba(oh)2 0,08M thu được dd có ph =12 .tính V
2 câu trả lời
Đáp án:
Giải thích các bước giải:
nKOH=0,04V(mol)
nBa(OH)2=0,08V(mol)
⇒nOH−=0,04V+0,08V.2=0,2V(mol)
nH+=nHCl=0,04.0,75=0,03(mol)
H++OH−→H2O
0,03 0,03 (mol)
⇒nOH− dư=0,2V−0,03(mol)
Mặt khác :
[OH− dư]=10−(14−12)=0,01M
⇒nOH− dư=0,01.(0,04+0,001V)(mol)
⇒0,2V−0,03=0,01.(0,04+0,001V)
⇒V=0,152(ml)
Câu hỏi trong lớp
Xem thêm