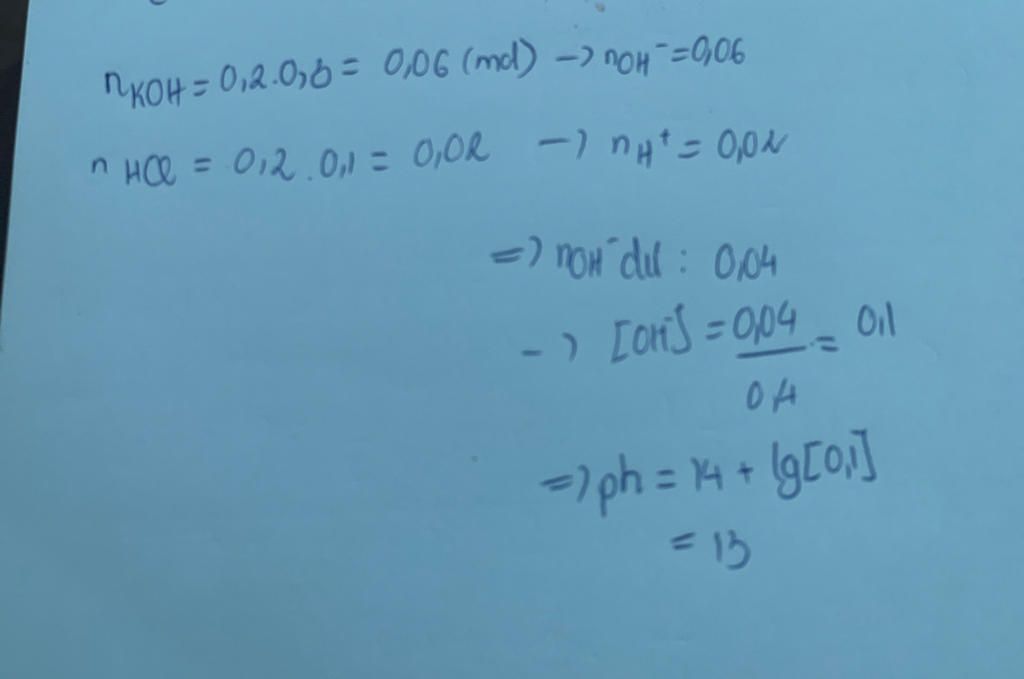Cho 200 ml dung dịch KOH 0,3M tác dụng với 200 ml dung dịch HCl 0,1M. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch có pH bằng
2 câu trả lời
Đáp án:
$pH=13$
Giải thích các bước giải:
$n_{OH^-}=n_{KOH}=0,2.0,3=0,06(mol)\\ n_{H^+}=n_{HCl}=0,1.0,2=0,02(mol)\\ H^++OH^-\to H_2O\\ Ta\ có\ n_{H^+}<n_{OH^-}\\ \Rightarrow OH^-\ dư\\ n_{OH^-\ dư}=0,04(Mol)\\ [OH^-]=\dfrac{0,04}{0,2+0,2}=0,1(mol)\\ \Rightarrow pH=14+\log([OH^-])=13$