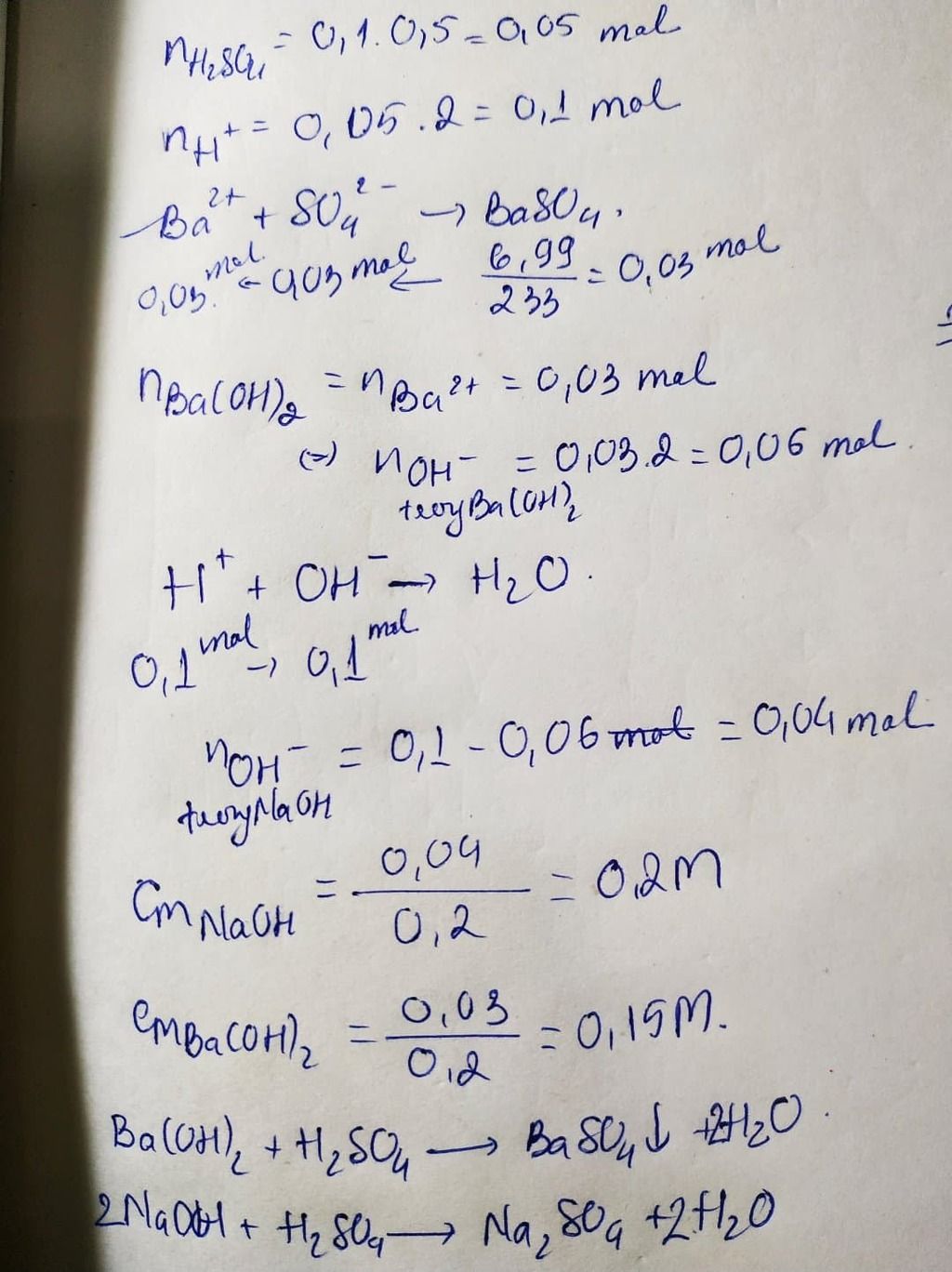cho 100ml h2so4 0,5M tác dụng vừa đủ với 200ml hỗn hợp gồm 2 bazo naoh và ba(oh)2 sau phản ứng thu được 6,99g kết tủa . tính nồn độ mol/l của 2 bazo trong hon hợp ban đâu, viết PTHH phản ứng xảy ra
2 câu trả lời
Đáp án: CM Ba(OH)2= 0.15M; CM NaOH= 0.2M
Giải thích các bước giải: n H2SO4= 0.5 ×0.1=0.05 mol; nBaSO4= 6.99/233= 0.03 mol
PTHH: H2SO4+ Ba(OH)2 →BaSO4 ↓ +2 H2O
0.03 ← 0.03 0.03
H2SO4+ 2NaOH → Na2SO4+2 H2O
0.02 → 0.04
CM Ba(OH)2= 0.03/0.2=0.15 M
CM NaOH= 0.04/ 0.2= 0.2M