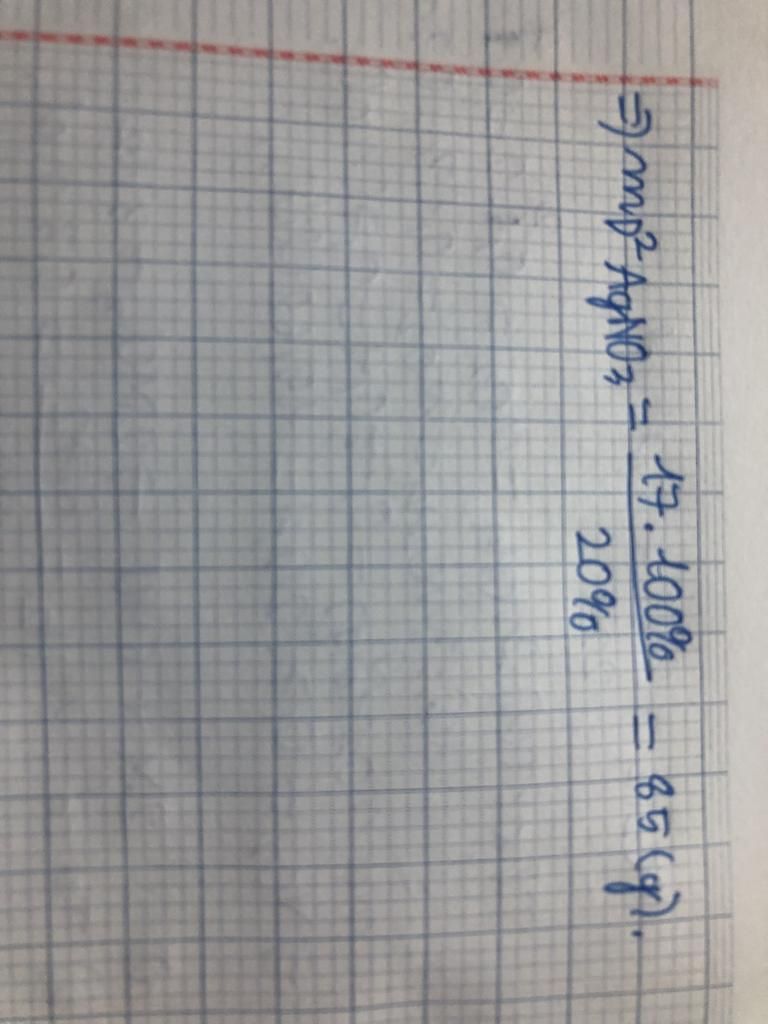Ngâm 1 lá đồng vào dung dịch AgNO3 20%. Sau phản ứng thu được dung dịch đồng(II) nitrat Cu(NO3)2 và 10,8 g Ag. Biết AgNO3 phản ứng hết. a. Viết phương trình phản ứng. b. Tính khối lượng dung dịch AgNO3 20% đã tham gia phản ứng.
2 câu trả lời
Giải thích các bước giải:
$nAg=$ `(10,8)/(108)` $=0,1mol$
a/. PTHH:
$2AgNO_3+Cu→Cu(NO_3)_2 +2Ag$
0,1 0,1 (mol)
b/. Theo phương trình, ta có:
$nAgNO_3=nAg=0,1mol$
$mAgNO_3=0,1.170=17g$
$mddAgNO_3=$ `(17)/(20%)` $=85g$