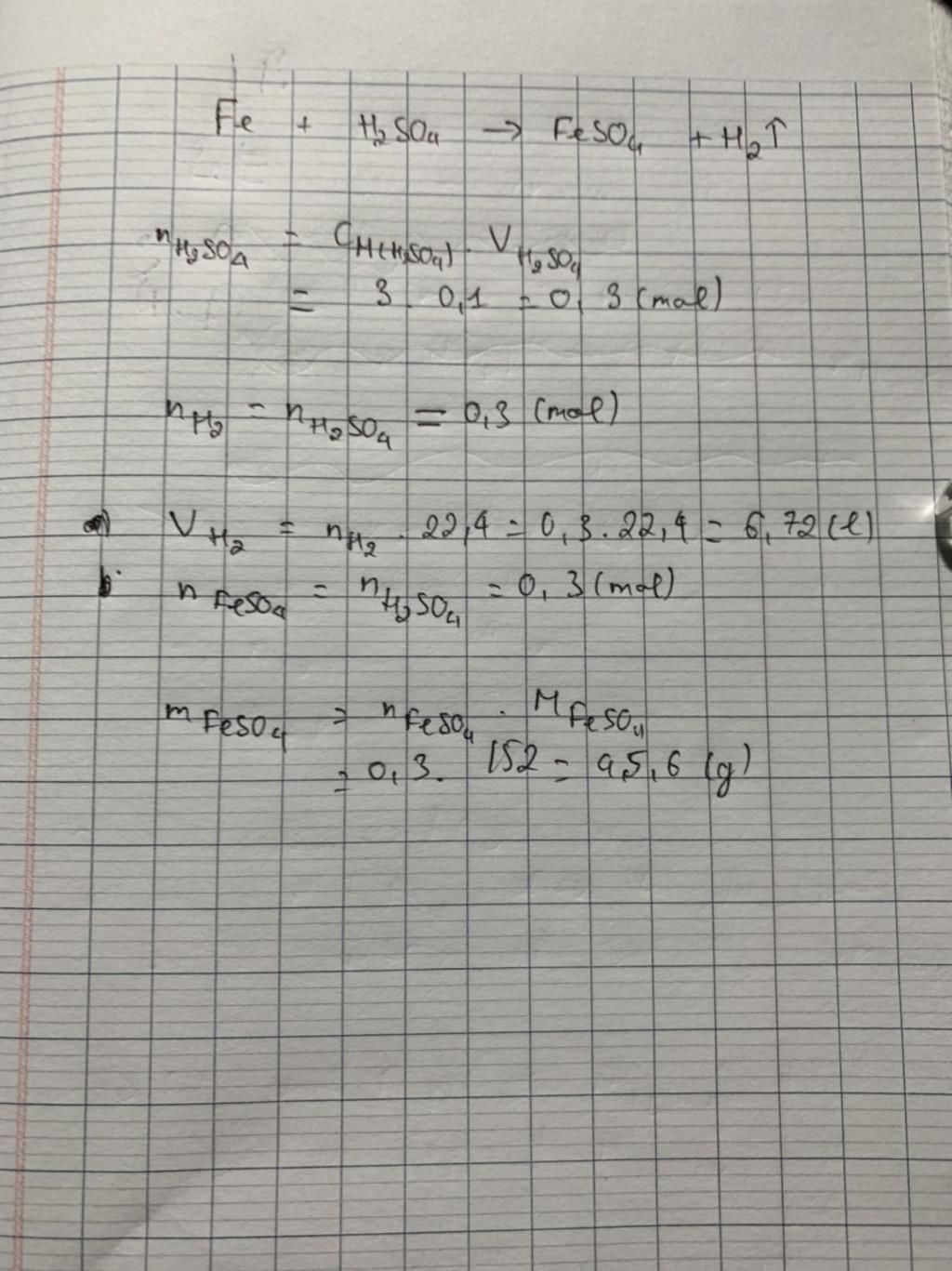Hòa tan hoàn toàn Fe vào 100ml dung dịch axit sunfuric (H2SO4) 3M. Tính: a/ Thể tích khí H2 thu được (đktc) b/ Khối lượng muối sinh ra? Giúp mình gấp ạ ! mình cảm ơn
2 câu trả lời
Đáp án+giải thích các bước giải:
a, Đổi 100 (ml)=0,1(l)
Số mol của `H_2SO_4` trong 100ml dung dịch `H_2SO_4` 3M là:
`n_{H_2SO_4}=C_M . V(l) = 3.0,1=0,3(mol)`
PTHH: `Fe + H_2SO_4 → FeSO_4 + H_2↑`
Tỉ lệ mol đề: 1 1 1 1
Tỉ lệ mol pt: 0,3 ------------------> 0,3
Thể tích khí `H_2` thu được (đktc) là:
`V_{H_2}=n.22,4=0,3.22,4=6,72(l)`
b, Theo PTHH trên ta có: `n_{H_2SO_4}=n_{FeSO_4}=0,3(mol)`
Khối lượng muối `(FeSO_4)` sinh ra là:
`m=n.M=0,3.152=45,6(g)`
Vậy...
Câu hỏi trong lớp
Xem thêm