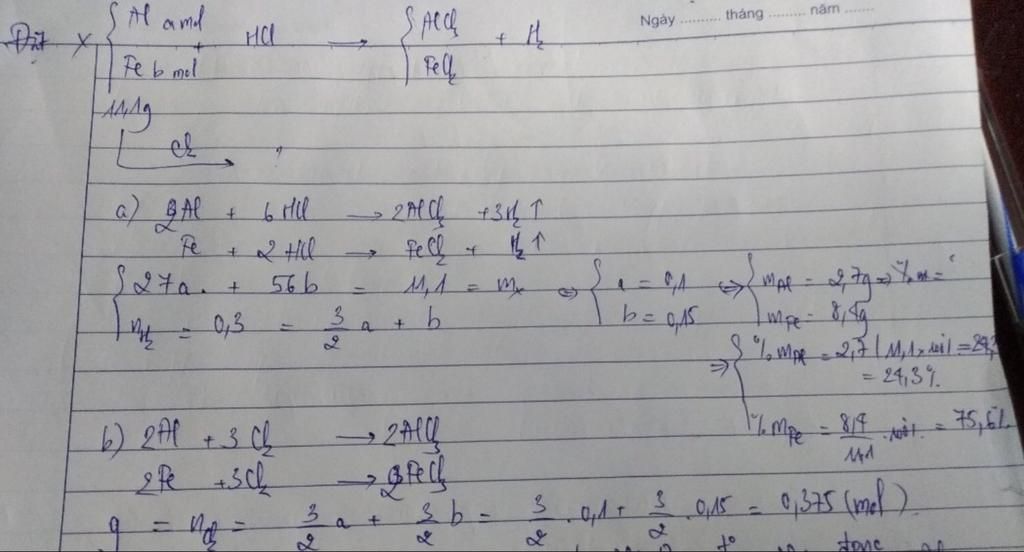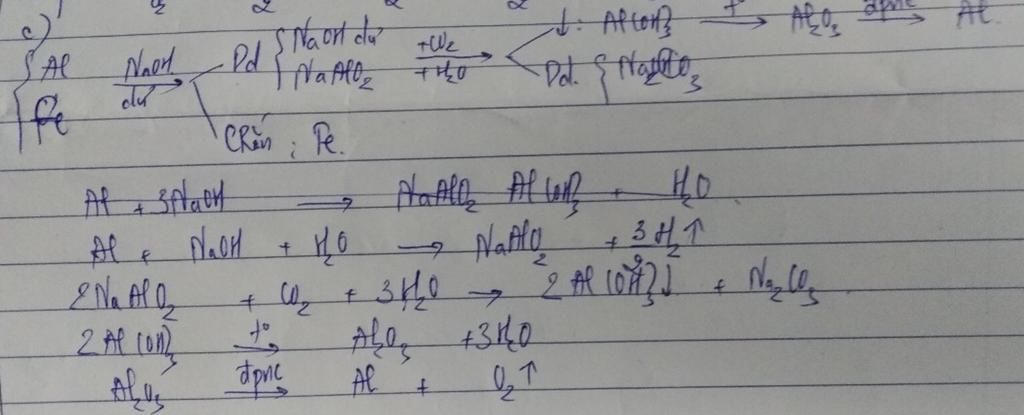C2: Hòa tan hoàn toàn 11,1 gam hỗn hợp X gồm Al và Fe bằng 1 lượng dư dd HCl, thu được 6,72 lít khí H2 (đktc) a. Viết PTHH của các pư xảy ra và tính phần trăm khối lượng của từng chất trong X b) Khi cho 11,1 gam X pư hết với khí Cl2(dư) thì có q mol Cl2 tham gia pư. Tính giá trị của q c) Bằng phương pháp hóa học hãy trình bày sơ đồ tách riêng kim loại ra khỏi hỗn hợp X
2 câu trả lời
Giải thích các bước giải:
a/. Đổi $672ml=0,672lít$
Gọi $x$ là số mol của $Al$; $y$ là số mol của $Fe$ trong hỗn hợp
PTHH:
$2Al+6HCl→2AlCl_3+3H_2↑$
x 1,5x (mol)
$Fe+2HCl→FeCl_2+H_2↑$
y y (mol)
Theo phương trình, ta có:
$27x+56y=11,1$ (1)
$1,5x+y=0,3$ (2)
Từ (1) và (2) ⇒ $x=0,1mol$ ; $y=0,15mol$
$mAl=0,1.27=2,7g$
$mFe=11,1-2,7=8,4g$
⇒ % $mAl=$ `(2,7)/(11,1)` $.100$ % $≈24,32$%
⇒ % $mAl=100$% $−24,32$% $=75,68$%
b/. PTHH:
$2Al+3Cl_2→2AlCl_3$
0,1 0,15 (mol)
$2Fe+3Cl_2→2FeCl_3$
0,15 0,225 (mol)
Ta có:
$p=nCl_2=0,15+0,225=0,375mol$
c/. Dung dịch $X$ gồm có: $Al$ và $Fe$
+ Dùng nam châm: nam châm sẽ hút sắt ra khỏi hỗn hợp $X$, Kim loại còn lại là $Al$